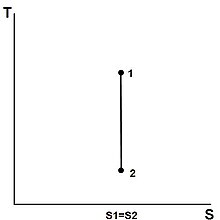
Procesul izentropic - Isentropic process
| Termodinamica |
|---|

|
În termodinamică , un proces izentropic este un proces termodinamic idealizat , care este atât adiabatic, cât și reversibil . De lucru transferurile ale sistemului sunt fricțiuni, și nu există nici un transfer net de energie termică sau materie. Un astfel de proces idealizat este util în inginerie ca model și bază de comparație pentru procese reale. Acest lucru este idealizat deoarece procesele reversibile nu apar în realitate; gândirea la un proces atât adiabatic, cât și reversibil ar arăta că entropiile inițiale și finale sunt aceleași, astfel, motivul pentru care este numit izentrop (entropia nu se schimbă). Procesele termodinamice sunt denumite pe baza efectului pe care l-ar avea asupra sistemului (ex. Izovolumetric: volum constant, izentalpic: entalpie constantă). Chiar dacă în realitate nu este neapărat posibil să se realizeze un proces izentropic, unele pot fi aproximate ca atare.
Cuvântul „izentrop” poate fi interpretat într-un alt mod, deoarece sensul său este deductibil din etimologia sa . Înseamnă un proces în care entropia sistemului rămâne neschimbată; așa cum am menționat, acest lucru ar putea apărea dacă procesul este atât adiabatic, cât și reversibil. Totuși, acest lucru s-ar putea întâmpla și într-un sistem în care munca efectuată asupra sistemului include frecare internă a sistemului, iar căldura este retrasă din sistem doar în cantitatea potrivită pentru a compensa fricțiunea internă, astfel încât să lase entropia neschimbată. Cu toate acestea, în raport cu universul, entropia universului ar crește ca urmare, în acord cu a doua lege a termodinamicii.
fundal
A doua lege a termodinamicii afirmă că
unde este cantitatea de energie pe care o câștigă sistemul prin încălzire, este temperatura mediului înconjurător și este schimbarea entropiei. Semnul egal se referă la un proces reversibil , care este o limită teoretică idealizată imaginată, care nu are loc niciodată în realitatea fizică, cu temperaturi esențial egale ale sistemului și ale împrejurimilor. Pentru un proces izentropic, dacă este și reversibil, nu există transfer de energie ca căldură deoarece procesul este adiabatic ; δQ = 0. În schimb, dacă procesul este ireversibil, se produce entropie în cadrul sistemului; în consecință, pentru a menține entropia constantă în cadrul sistemului, energia trebuie eliminată simultan din sistem sub formă de căldură.
Pentru procesele reversibile, se efectuează o transformare izentropică prin „izolarea” termică a sistemului de împrejurimile sale. Temperatura este variabila conjugată termodinamică la entropie, astfel procesul conjugat ar fi un proces izoterm , în care sistemul este „conectat” termic la o baie de căldură cu temperatură constantă.
Procese izentropice în sistemele termodinamice
Entropia unei mase date nu se schimbă în timpul unui proces care este intern reversibil și adiabatic. Un proces în care entropia rămâne constantă se numește proces izentropic, scris sau . Câteva exemple de dispozitive termodinamice teoretic izentrope sunt pompele , compresoarele de gaz , turbine , duze și difuzoare .
Eficiența izentropică a dispozitivelor cu flux constant în sistemele termodinamice
Majoritatea dispozitivelor cu flux constant funcționează în condiții adiabatice, iar procesul ideal pentru aceste dispozitive este procesul izentropic. Parametrul care descrie cât de eficient se apropie un dispozitiv de un dispozitiv izentropic corespunzător se numește eficiență izentropă sau adiabatică.
Eficiența izentropică a turbinelor:
Eficiența izentropică a compresoarelor:
Eficiența izentropică a duzelor:
Pentru toate ecuațiile de mai sus:
- este entalpia specifică la starea de intrare,
- este entalpia specifică la starea de ieșire pentru procesul efectiv,
- este entalpia specifică la starea de ieșire pentru procesul izentropic.
Dispozitive izentropice în cicluri termodinamice
| Ciclu | Pas isentropic | Descriere |
|---|---|---|
| Ciclul ideal Rankine | 1 → 2 | Compresie izentropică într-o pompă |
| Ciclul ideal Rankine | 3 → 4 | Expansiunea izentropică într-o turbină |
| Ciclul ideal Carnot | 2 → 3 | Expansiunea izentropică |
| Ciclul ideal Carnot | 4 → 1 | Compresie izentropică |
| Ciclul Otto ideal | 1 → 2 | Compresie izentropică |
| Ciclul Otto ideal | 3 → 4 | Expansiunea izentropică |
| Ciclul Diesel ideal | 1 → 2 | Compresie izentropică |
| Ciclul Diesel ideal | 3 → 4 | Expansiunea izentropică |
| Ciclul ideal Brayton | 1 → 2 | Compresie izentropică într-un compresor |
| Ciclul ideal Brayton | 3 → 4 | Expansiunea izentropică într-o turbină |
| Ciclul ideal de refrigerare prin compresie de vapori | 1 → 2 | Compresie izentropică într-un compresor |
| Ciclul ideal Lenoir | 2 → 3 | Expansiunea izentropică |
Notă: Ipotezele izentropice se aplică numai în cazul ciclurilor ideale. Ciclurile reale au pierderi inerente din cauza ineficiențelor compresorului și turbinei și a celei de-a doua legi a termodinamicii. Sistemele reale nu sunt cu adevărat izentrope, dar comportamentul izentropic este o aproximare adecvată pentru multe scopuri de calcul.
Fluxul izentropic
În dinamica fluidelor, un flux izentropic este un flux fluid care este atât adiabatic, cât și reversibil. Adică, nu se adaugă căldură fluxului și nu se produc transformări de energie din cauza frecării sau a efectelor disipative . Pentru un flux izentropic al unui gaz perfect, pot fi derivate mai multe relații pentru a defini presiunea, densitatea și temperatura de-a lungul unei linii aeriene.
Rețineți că energia poate fi schimbată cu fluxul într-o transformare izentropică, atâta timp cât nu se întâmplă ca schimb de căldură. Un exemplu de astfel de schimb ar fi o expansiune sau compresie izentropică care presupune munca efectuată pe sau prin flux.
Pentru un flux izentropic, densitatea entropiei poate varia între diferite linii de curgere. Dacă densitatea entropiei este aceeași peste tot, atunci se spune că fluxul este homentropic .
Derivarea relațiilor izentropice
Pentru un sistem închis, schimbarea totală a energiei unui sistem este suma muncii efectuate și a căldurii adăugate:
Lucrarea reversibilă efectuată pe un sistem prin schimbarea volumului este
unde este presiunea , și este volumul . Modificarea entalpiei ( ) este dată de
Apoi pentru un proces care este atât reversibil, cât și adiabatic (adică nu are loc transfer de căldură) , și astfel Toate procesele adiabatice reversibile sunt izentrope. Acest lucru duce la două observații importante:
Apoi, se poate calcula o mare parte pentru procesele izentropice ale unui gaz ideal. Pentru orice transformare a unui gaz ideal, este întotdeauna adevărat că
- , și
Folosind rezultatele generale derivate mai sus pentru și , apoi
Deci, pentru un gaz ideal, raportul capacității termice poate fi scris ca
Pentru un gaz perfect caloric este constant. Prin urmare, integrând ecuația de mai sus, presupunând un gaz perfect caloric, obținem
acesta este,
Folosind ecuația de stare pentru un gaz ideal ,,
(Dovadă: dar nR = constantă în sine, deci .)
de asemenea, pentru constantă (pe mol),
- și
Astfel, pentru procesele izentropice cu un gaz ideal,
- sau
Tabelul relațiilor izentropice pentru un gaz ideal
Derivat de la
Unde:
- = presiune,
- = volum,
- = raportul de călduri specifice = ,
- = temperatura,
- = masa,
- = constanta gazului pentru gazul specific = ,
- = constanta de gaz universala,
- = greutatea moleculară a gazului specific,
- = densitate,
- = căldură specifică la presiune constantă,
- = căldură specifică la volum constant.
Vezi si
Note
Referințe
- Van Wylen, G. J. și Sonntag, R. E. (1965), Fundamentals of Classical Thermodynamics , John Wiley & Sons, Inc., New York. Catalog Catalog Catalog Library Library: 65-19470