Cancer de plamani -Lung cancer
| Cancer de plamani | |
|---|---|
| Alte nume | Carcinom pulmonar |
 | |
| O radiografie toracică care arată o tumoare în plămân (marcată cu săgeată) | |
| Specialitate | Oncologie , pneumologie |
| Simptome | Tuse (inclusiv tuse cu sânge ), scădere în greutate , dificultăți de respirație , dureri în piept |
| Debut obișnuit | ~70 de ani |
| Tipuri | Carcinom pulmonar cu celule mici (SCLC), carcinom pulmonar fără celule mici (NSCLC) |
| Factori de risc | |
| Metoda de diagnosticare | Imagistica medicală , biopsie tisulară |
| Prevenirea | Nu fumați, evitați gazul radon , azbest , fumatul pasiv sau alte forme de expunere la poluarea aerului . |
| Tratament | Chirurgie , chimioterapie , radioterapie |
| Prognoză | Rata de supraviețuire la cinci ani : 10 până la 20% (majoritatea țărilor), 33% (Japonia), 27% (Israel), 25% (Republica Coreea) |
| Frecvență | 3,3 milioane afectate începând cu 2015 |
| Decese | 1,8 milioane (2020) |
Cancerul pulmonar , cunoscut și sub denumirea de carcinom pulmonar , deoarece aproximativ 98–99% din toate cancerele pulmonare sunt carcinoame, este o tumoare pulmonară malignă caracterizată prin creșterea necontrolată a celulelor în țesuturile pulmonare . Carcinoamele pulmonare derivă din celule maligne transformate care provin ca celule epiteliale sau din țesuturi compuse din celule epiteliale. Alte tipuri de cancer pulmonar, precum sarcoamele rare ale plămânului, sunt generate de transformarea malignă a țesuturilor conjunctive (adică nervi, grăsimi, mușchi, oase), care provin din celulele mezenchimale. Limfoamele și melanoamele (din liniile de celule limfoide și melanocite) pot duce, de asemenea, rareori la cancer pulmonar.
În timp, această creștere necontrolată se poate răspândi dincolo de plămâni – fie prin extensie directă, prin intrarea în circulația limfatică, fie prin răspândire hematogenă, transmisă prin sânge – procesul numit metastază – în țesutul din apropiere sau în alte părți mai îndepărtate ale corpului. Majoritatea cancerelor care debutează în plămâni, cunoscute sub denumirea de cancere pulmonare primare, sunt carcinoame . Cele două tipuri principale sunt carcinomul pulmonar cu celule mici (SCLC) și carcinomul pulmonar fără celule mici (NSCLC). Cele mai frecvente simptome sunt tusea (inclusiv tusea cu sânge ), pierderea în greutate, dificultăți de respirație și dureri în piept .
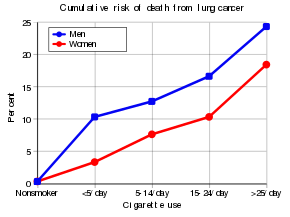
Marea majoritate (85%) a cazurilor de cancer pulmonar se datorează fumatului pe termen lung . Aproximativ 10-15% din cazuri apar la persoane care nu au fumat niciodată. Aceste cazuri sunt adesea cauzate de o combinație de factori genetici și expunerea la gaz radon , azbest , fum pasiv sau alte forme de poluare a aerului . Cancerul pulmonar poate fi observat pe radiografiile toracice și pe tomografia computerizată (CT). Diagnosticul este confirmat prin biopsie , care este de obicei efectuată prin bronhoscopie sau ghidare CT.
Metoda majoră de prevenire este evitarea factorilor de risc, inclusiv fumatul și poluarea aerului. Tratamentul și rezultatele pe termen lung depind de tipul de cancer, stadiul (gradul de răspândire) și starea generală de sănătate a persoanei. Majoritatea cazurilor nu sunt vindecabile. Tratamentele comune includ chirurgie , chimioterapie și radioterapie . NSCLC este uneori tratat prin intervenție chirurgicală, în timp ce SCLC răspunde de obicei mai bine la chimioterapie și radioterapie.
La nivel mondial, în 2020, cancerul pulmonar a apărut la 2,2 milioane de oameni și a dus la 1,8 milioane de decese. Este cea mai frecventă cauză a decesului cauzat de cancer atât la bărbați, cât și la femei. Cea mai frecventă vârstă la diagnosticare este de 70 de ani. În majoritatea țărilor, rata de supraviețuire la cinci ani este de aproximativ 10 până la 20%, în timp ce în Japonia este de 33%, în Israel de 27% și în Republica Coreea de 25%. Rezultatele sunt de obicei mai rele în lumea în curs de dezvoltare.
semne si simptome
Semnele și simptomele care pot sugera cancer pulmonar includ:
- Simptome respiratorii: tuse , tuse cu sânge , respirație șuierătoare sau dificultăți de respirație
- Simptome sistemice: scădere în greutate, slăbiciune , febră sau lovire a unghiilor
- Simptome datorate presării masei canceroase asupra structurilor adiacente: durere toracică , durere osoasă , obstrucție a venei cave superioare sau dificultăți la înghițire
Dacă cancerul crește în căile respiratorii , acesta poate obstrucționa fluxul de aer cauzând dificultăți de respirație. Obstrucția poate duce, de asemenea, la acumularea de secreții în spatele blocajului și poate crește riscul de pneumonie .
Multe dintre simptomele cancerului pulmonar (apetit scăzut, scădere în greutate, febră, oboseală) nu sunt specifice. La mulți oameni, cancerul sa răspândit deja dincolo de locul inițial în momentul în care au simptome și solicită asistență medicală. Simptomele care sugerează prezența bolii metastatice includ pierderea în greutate, dureri osoase și simptome neurologice (dureri de cap, leșin , convulsii sau slăbiciune a membrelor). Locurile comune de răspândire includ creierul, oasele, glandele suprarenale , plămânul opus, ficatul , pericardul și rinichii . Aproximativ 10% dintre persoanele cu cancer pulmonar nu au simptome la diagnostic; aceste tipuri de cancer se găsesc întâmplător pe radiografia toracică de rutină .
În funcție de tipul tumorii, fenomenele paraneoplazice – simptome care nu se datorează prezenței locale a cancerului – pot atrage inițial atenția asupra bolii. În cancerul pulmonar, aceste fenomene pot include hipercalcemie , sindromul hormonului antidiuretic inadecvat (urină concentrată anormal și sânge diluat), producția de ACTH ectopică sau sindromul miastenic Lambert-Eaton (slăbiciune musculară datorată autoanticorpilor ). Tumorile din partea superioară a plămânului , cunoscute sub numele de tumori Pancoast , pot invada partea locală a sistemului nervos simpatic , ducând la sindromul Horner (căderea pleoapei și a unei pupile mici pe acea parte), precum și afectarea plexului brahial . .
Cauze
Cancerul se dezvoltă după leziuni genetice ale ADN- ului și modificări epigenetice . Aceste modificări afectează funcțiile normale ale celulei , inclusiv proliferarea celulară , moartea celulară programată ( apoptoza ) și repararea ADN-ului . Pe măsură ce se acumulează mai multe daune, crește riscul de cancer.
Fumat
Fumatul de tutun este de departe principalul contributor la cancerul pulmonar. Fumul de țigară conține cel puțin 73 de agenți cancerigeni cunoscuți , inclusiv benzo[ a ]piren , NNK , 1,3-butadienă și un izotop radioactiv al poloniului – poloniu-210 . În lumea dezvoltată, 90% din decesele cauzate de cancer pulmonar la bărbați și 70% dintre cele la femei în cursul anului 2000 au fost atribuite fumatului. Fumatul reprezintă aproximativ 85% din cazurile de cancer pulmonar. Vapoarea poate fi un factor de risc pentru cancerul pulmonar, dar mai puțin decât cel al țigărilor, și sunt necesare cercetări suplimentare din cauza duratei de timp care poate dura pentru ca cancerul pulmonar să se dezvolte în urma expunerii la agenți cancerigeni.
Fumatul pasiv – inhalarea fumului de la fumatul altuia – este o cauză a cancerului pulmonar la nefumători. Un fumător pasiv poate fi definit ca o persoană care trăiește sau lucrează cu un fumător. Studiile din SUA, Marea Britanie și alte țări europene au arătat în mod constant un risc semnificativ crescut în rândul celor expuși la fumatul pasiv. Riscul de a dezvolta cancer pulmonar crește cu 25-28%. Investigațiile privind fumul secundar (componenta principală a fumului pasiv; aproximativ 85%) sugerează că este mai periculos decât fumul direct principal.
Fumul de marijuana conține mulți dintre aceiași agenți cancerigeni ca cei găsiți în fumul de tutun, dar efectul fumatului de canabis asupra riscului de cancer pulmonar nu este clar. O analiză din 2013 nu a găsit un risc crescut de la utilizarea ușoară la moderată. O analiză din 2014 a constatat că fumatul de canabis a dublat riscul de cancer pulmonar, deși în multe țări canabisul este în mod obișnuit amestecat cu tutun.
Gazul radon
Radonul este un gaz incolor și inodor generat de descompunerea radiului radioactiv , care, la rândul său, este produsul de descompunere al uraniului , găsit în scoarța terestră . Produșii de degradare prin radiații ionizează materialul genetic, provocând mutații care uneori devin canceroase. Radonul este a doua cea mai frecventă cauză de cancer pulmonar în SUA, provocând aproximativ 21.000 de decese în fiecare an. Riscul crește cu 8–16% pentru fiecare 100 Bq / m³ de creștere a concentrației de radon. Nivelurile de gaz radon variază în funcție de localitate și de compoziția solului și a rocilor subiacente. Aproximativ una din 15 case din SUA are niveluri de radon peste limita recomandată de 4 picocuri per litru (pCi/l) (148 Bq/m³).
Azbest
Azbestul poate provoca o varietate de boli pulmonare, cum ar fi cancerul pulmonar. Fumatul de tutun și expunerea la azbest împreună au efecte sinergice asupra dezvoltării cancerului pulmonar. La fumătorii care lucrează cu azbest, riscul de cancer pulmonar este crescut de 45 de ori comparativ cu populația generală. De asemenea, azbestul poate provoca cancer de pleura , numit mezoteliom – care de fapt este diferit de cancerul pulmonar.
Poluarea aerului
Poluanții aerului exterior , în special substanțele chimice eliberate din arderea combustibililor fosili , cresc riscul de cancer pulmonar. Particulele fine (PM 2,5 ) și aerosolii de sulfat , care pot fi eliberați în gazele de evacuare din trafic , sunt asociate cu un risc ușor crescut. Pentru dioxidul de azot , o creștere incrementală de 10 părți pe miliard crește riscul de cancer pulmonar cu 14%. Se estimează că poluarea aerului exterior cauzează 1-2% din cancerele pulmonare.
Dovezile provizorii susțin un risc crescut de cancer pulmonar din cauza poluării aerului din interior în legătură cu arderea lemnului , a cărbunelui , a bălegarului sau a reziduurilor de recoltă pentru gătit și încălzire. Femeile care sunt expuse la fumul de cărbune din interior au un risc de aproximativ dublu, iar multe dintre produsele secundare ale arderii biomasei sunt cancerigene cunoscute sau suspectate. Acest risc afectează aproximativ 2,4 miliarde de oameni din întreaga lume și se crede că are ca rezultat 1,5% din decesele cauzate de cancer pulmonar.
Genetica
Aproximativ 8% din cazurile de cancer pulmonar sunt cauzate de factori ereditari (genetici). La rudele persoanelor care sunt diagnosticate cu cancer pulmonar, riscul este dublat, probabil din cauza unei combinații de gene . Polimorfismele de pe cromozomii 5, 6 și 15 au fost identificate și sunt asociate cu un risc crescut de cancer pulmonar. Polimorfismele cu un singur nucleotide ale genelor care codifică receptorul nicotinic de acetilcolină (nAChR) – CHRNA5 , CHRNA3 și CHRNB4 – sunt dintre cele asociate cu un risc crescut de cancer pulmonar, precum și RGS17 – o genă care reglează semnalizarea proteinei G. Studiile genetice mai noi au identificat 18 loci de susceptibilitate care dobândesc semnificație la nivel de genom. Acești loci evidențiază o eterogenitate în susceptibilitatea genetică între subtipurile histologice de cancer pulmonar, identificând din nou receptorii nicotinici colinergici, de exemplu CHRNA2.
Alte cauze
Numeroase alte substanțe, ocupații și expuneri la mediu au fost legate de cancerul pulmonar. Agenția Internațională pentru Cercetare a Cancerului afirmă că există „dovezi suficiente” pentru a demonstra că următoarele sunt cancerigene în plămâni:
- Unele metale ( producția de aluminiu , compuși de cadmiu și cadmiu, compuși de crom (VI) , compuși de beriliu și beriliu, bază de fier și oțel , compuși de nichel , arsen și compuși anorganici de arsen și exploatare subterană a hematitei )
- Unele produse ale arderii (combustie incompletă, cărbune (emisii în interior de la arderea cărbunelui casnic), gazeificarea cărbunelui , smoală de gudron de cărbune , producția de cocs , funingine și evacuarea motorului diesel )
- Radiații ionizante ( raze X și gamma )
- Unele gaze toxice ( eter metilic (grad tehnic) și bis-(clorometil)eter , muștar cu sulf , MOPP (amestec vincristină-prednison-azot muștar-procarbazină ) și vapori de la vopsire )
- Producția de cauciuc și praf de silice cristalină
- O mică creștere a riscului de cancer pulmonar este observată la persoanele afectate de scleroză sistemică .
Patogeneza
Similar cu multe alte tipuri de cancer, cancerul pulmonar este inițiat fie prin activarea oncogenelor , fie prin inactivarea genelor supresoare de tumori . Agenții cancerigeni provoacă mutații în aceste gene care induc dezvoltarea cancerului.
Mutațiile proto-oncogenei K-ras contribuie la aproximativ 10-30% din adenocarcinoamele pulmonare . Aproape 4% dintre carcinoamele pulmonare fără celule mici implică o genă de fuziune a tirozin kinazei EML4-ALK .
Modificările epigenetice , cum ar fi alterarea metilării ADN-ului , modificarea cozii histonelor sau reglarea microARN pot duce la inactivarea genelor supresoare de tumori. Foarte important, celulele canceroase dezvoltă rezistență la stresul oxidativ , ceea ce le permite să reziste și să exacerbeze condițiile inflamatorii care inhibă activitatea sistemului imunitar împotriva tumorii.
Receptorul factorului de creștere epidermic (EGFR) reglează proliferarea celulară, apoptoza , angiogeneza și invazia tumorii. Mutațiile și amplificarea EGFR sunt frecvente în NSCLC și oferă baza pentru tratamentul cu inhibitori EGFR. Her2/neu este afectată mai rar. Alte gene care sunt adesea mutate sau amplificate includ c-MET , NKX2-1 , LKB1 , PIK3CA și BRAF .
Liniile celulare de origine nu sunt pe deplin înțelese. Mecanismul poate implica activarea anormală a celulelor stem . În căile respiratorii proximale, celulele stem care exprimă keratina 5 sunt mai susceptibile de a fi afectate, ducând de obicei la carcinom pulmonar cu celule scuamoase . În căile respiratorii medii, celulele stem implicate includ celule club și celule neuroepiteliale care exprimă proteina secretorie a celulelor club . SCLC poate proveni din aceste linii celulare sau celule neuroendocrine și poate exprima CD44 .
Metastaza cancerului pulmonar necesită trecerea de la tipul de celule epiteliale la celulă mezenchimală . Acest lucru poate apărea prin activarea căilor de semnalizare, cum ar fi Akt / GSK3Beta , MEK-ERK , Fas și Par6.
Diagnostic


Efectuarea unei radiografii toracice (raze X) este unul dintre primii pași de investigație dacă o persoană raportează simptome care pot sugera cancer pulmonar. Radiografia poate dezvălui o masă evidentă, lărgirea mediastinului (sugestivă de răspândire la ganglionii limfatici de acolo), atelectazie (colaps pulmonar), consolidare ( pneumonie ) sau revărsat pleural . Tomografia computerizată (CT) a toracelui este adesea folosită pentru diagnostic și poate dezvălui o masă spiculată care este foarte sugestivă pentru cancer pulmonar. Imagistica CT este, de asemenea, utilizată pentru a oferi mai multe informații despre tipul și amploarea bolii. Biopsia bronhoscopică sau ghidată de CT este adesea utilizată pentru a preleva tumora pentru histopatologie .
Cancerul pulmonar poate apărea adesea ca un nodul pulmonar solitar pe o radiografie toracică. Cu toate acestea, diagnosticul diferențial este larg și multe alte boli pot da, de asemenea, acest aspect, inclusiv cancerul metastatic, hamartoamele și granuloamele infecțioase cauzate de tuberculoză , histoplasmoză sau coccidioidomicoză . Cancerul pulmonar poate fi, de asemenea, o descoperire accidentală , ca un nodul pulmonar solitar pe o radiografie toracică sau o scanare CT făcută dintr-un motiv care nu are legătură. Diagnosticul definitiv al cancerului pulmonar se bazează pe examinarea histologică a țesutului suspect în contextul caracteristicilor clinice și radiologice.
Ghidurile de practică clinică recomandă frecvențe specifice (intervalele de timp sugerate între teste) pentru supravegherea nodulilor pulmonari. Nu se sugerează ca imagistica CT să fie utilizată mai mult sau mai frecvent decât este indicat în ghidurile clinice, deoarece orice supraveghere suplimentară expune oamenii la radiații crescute și este costisitoare.
Clasificare
| Tip histologic | Incidență la 100.000 pe an |
|---|---|
| Toate tipurile | 66,9 |
| Adenocarcinom | 22.1 |
| Carcinom cu celule scuamoase | 14.4 |
| Carcinom cu celule mici | 9.8 |
Cancerele pulmonare sunt clasificate în funcție de tipul histologic . Această clasificare este importantă pentru a determina atât managementul, cât și pentru prezicerea rezultatelor bolii. Cancerele pulmonare sunt carcinoame – afecțiuni maligne care apar din celulele epiteliale . Carcinoamele pulmonare sunt clasificate în funcție de dimensiunea și aspectul celulelor maligne văzute de un histopatolog la microscop. În scopuri terapeutice, se disting două clase largi: carcinomul pulmonar non-microcelular (NSCLC) și carcinomul pulmonar cu celule mici (SCLC).
Carcinom pulmonar fără celule mici
Cele trei subtipuri principale de NSCLC sunt adenocarcinomul , carcinomul cu celule scuamoase și carcinomul cu celule mari . Subtipurile rare includ adenocarcinomul enteric pulmonar .
Aproape 40% dintre cancerele pulmonare sunt adenocarcinoame, care provin de obicei din țesutul pulmonar periferic. Deși majoritatea cazurilor de adenocarcinom sunt asociate cu fumatul, este, de asemenea, cea mai frecventă formă de cancer pulmonar în rândul persoanelor care au fumat mai puțin de 100 de țigări în timpul vieții („nu-fumători niciodată”) și al foștilor fumători cu un istoric modest de fumat. Un subtip de adenocarcinom, carcinomul bronhioloalveolar , este mai frecvent la femeile care nu fumează niciodată și poate avea o supraviețuire mai bună pe termen lung.
Carcinomul cu celule scuamoase cauzează aproximativ 30% din cancerele pulmonare. Ele apar de obicei în apropierea căilor respiratorii mari. O cavitate goală și moartea celulară asociată se găsesc de obicei în centrul tumorii.
Aproximativ 10 până la 15% dintre cancerele pulmonare sunt carcinom cu celule mari. Acestea sunt numite astfel deoarece celulele canceroase sunt mari, cu citoplasmă în exces, nuclei mari și nucleoli vizibili .
Carcinom pulmonar cu celule mici
În SCLC, celulele conțin granule neurosecretoare dense ( vezicule care conțin hormoni neuroendocrini ), care conferă acestei tumori o asociere cu sindrom endocrin sau paraneoplazic . Cele mai multe cazuri apar în căile respiratorii mai mari ( bronhiile primare și secundare ). Aproximativ 60-70% au o boală extinsă (care nu poate fi vizată într-un singur domeniu de radioterapie) la prezentare.
Alții
Sunt recunoscute patru subtipuri histologice principale, deși unele tipuri de cancer pot conține o combinație de diferite subtipuri, cum ar fi carcinomul adenosquamos . Subtipurile rare includ tumorile carcinoide , carcinoamele glandelor bronșice și carcinoamele sarcomatoide .
Metastaze
| Tip histologic | Napsin-A | TTF-1 |
|---|---|---|
| Carcinom cu celule scuamoase | Negativ | Negativ |
| Adenocarcinom | Pozitiv | Pozitiv |
| Carcinom cu celule mici | Negativ | Pozitiv |
Plămânii sunt un loc obișnuit pentru răspândirea tumorilor din alte părți ale corpului. Aceste tumori se numesc metastaze sau tumori secundare. Cea mai frecventă apariție la radiografia toracică este prezența unor noduli multipli în lobii inferiori.
De asemenea, cancerele pulmonare primare metastazează cel mai frecvent la creier, oase, ficat și glandele suprarenale . Imunocolorarea unei biopsii ajută de obicei la determinarea sursei inițiale. Prezența Napsin-A , TTF-1 , CK7 și CK20 ajută la confirmarea subtipului de carcinom pulmonar. SCLC care provine din celulele neuroendocrine poate exprima CD56 , moleculă de adeziune a celulelor neuronale , sinaptofizina sau cromogranina .
Înscenare
Stadializarea cancerului pulmonar este o evaluare a gradului de răspândire a cancerului din sursa inițială. Este unul dintre factorii care afectează atât prognosticul , cât și potențialul tratament al cancerului pulmonar.
Evaluarea stadializării NSCLC utilizează clasificarea TNM (tumora, nodul, metastaza). Aceasta se bazează pe dimensiunea tumorii primare, implicarea ganglionilor limfatici și metastazele la distanță.
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Folosind descriptorii TNM, se atribuie un grup, variind de la cancerul ocult, prin stadiile 0, IA (unu-A), IB, IIA, IIB, IIIA, IIIB și IV (patru). Acest grup de etape ajută la alegerea tratamentului și la estimarea prognosticului.
| TNM | Grup de scenă |
|---|---|
| T1a–T1b N0 M0 | in absenta |
| T2a N0 M0 | IB |
| T1a–T2a N1 M0 | IIA |
| T2b N0 M0 | |
| T2b N1 M0 | IIB |
| T3 N0 M0 | |
| T1a–T3 N2 M0 | IIIA |
| T3 N1 M0 | |
| T4 N0–N1 M0 | |
| N3 M0 | IIIB |
| T4 N2 M0 | |
| M1 | IV |
SCLC a fost în mod tradițional clasificat ca „stadiu limitat” (limitat la jumătate din torace și în sfera de aplicare a unui singur domeniu de radioterapie tolerabil ) sau „stadiu extins” (boală mai răspândită). Cu toate acestea, clasificarea și gruparea TNM sunt utile în estimarea prognosticului.
Atât pentru NSCLC, cât și pentru SCLC, cele două tipuri generale de evaluări de stadializare sunt stadializarea clinică și stadializarea chirurgicală. Stadializarea clinică se efectuează înainte de intervenția chirurgicală definitivă. Se bazează pe rezultatele studiilor imagistice (cum ar fi scanările CT și scanările PET ) și rezultatele biopsiei. Stadializarea chirurgicală este evaluată fie în timpul operației, fie după aceasta. Se bazează pe rezultatele combinate ale constatărilor chirurgicale și clinice, inclusiv prelevarea chirurgicală a ganglionilor limfatici toracici.
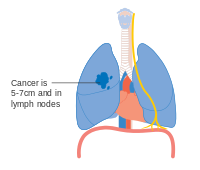
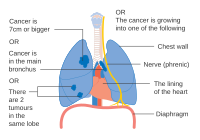
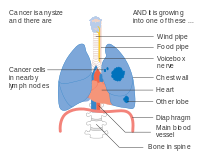
- Diagrame ale principalelor caracteristici ale punerii în scenă
O opțiune pentru cancerul pulmonar în stadiul IIB, cu T2b; dar dacă tumora se află la 2 cm de carină , acesta este stadiul 3
Prevenirea

Prevenirea fumatului și renunțarea la fumat sunt modalități eficiente de reducere a riscului de cancer pulmonar.
Interzicerea fumatului
În timp ce în majoritatea țărilor au fost identificați și interziși agenții cancerigeni industriali și domestici, fumatul de tutun este încă larg răspândit. Eliminarea fumatului este un obiectiv principal în prevenirea cancerului pulmonar, iar renunțarea la fumat este un instrument preventiv important în acest proces.
Intervențiile politice pentru a reduce fumatul pasiv în zonele publice, cum ar fi restaurantele și locurile de muncă, au devenit mai frecvente în multe țări occidentale . Bhutanul are o interdicție totală de fumat din 2005, în timp ce India a introdus o interdicție de fumat în public în octombrie 2008. Organizația Mondială a Sănătății a cerut guvernelor să instituie o interdicție totală a publicității pentru tutun pentru a împiedica tinerii să se apuce de fumat. Ei evaluează că astfel de interdicții au redus consumul de tutun cu 16% acolo unde au fost instituite.
Screening
Depistarea cancerului folosește teste medicale pentru a detecta boala la grupuri mari de oameni care nu prezintă simptome. Pentru persoanele cu risc crescut de a dezvolta cancer pulmonar, tomografia computerizată (CT) poate detecta cancerul și poate oferi persoanei opțiuni de a răspunde la acesta într-un mod care prelungește viața. Această formă de screening reduce șansa de deces din cauza cancerului pulmonar cu o cantitate absolută de 0,3% ( cantitate relativă de 20%). Persoanele cu risc ridicat sunt acele persoane cu vârsta cuprinsă între 55 și 74 de ani care au fumat zilnic o cantitate echivalentă dintr-un pachet de țigări timp de 30 de ani, inclusiv timpul în ultimii 15 ani.
Screening-ul CT este asociat cu o rată ridicată de teste fals pozitive , ceea ce poate duce la un tratament inutil. Pentru fiecare scanare pozitivă precisă există aproximativ 19 scanări fals pozitive. Alte preocupări includ expunerea la radiații și costul testării împreună cu urmărirea. Cercetările nu au descoperit că alte două teste disponibile - citologie de spută sau teste de screening cu radiografie toracică (CXR) - să aibă vreun beneficiu.
Grupul operativ al Serviciilor Preventive din Statele Unite recomandă screening-ul anual folosind CT cu doze mici la cei care au un istoric total de fumat de 30 de pachete-ani și au între 55 și 80 de ani, până când o persoană nu fumează de mai mult de 15 ani. Recomandarea lor îi exclude pe cei cu alte probleme de sănătate care ar face tratamentul cancerului pulmonar dacă nu ar fi găsit o opțiune. Serviciul Național de Sănătate Englez a reexaminat în 2014 dovezile pentru screening.
Alte strategii de prevenire
Utilizarea pe termen lung a suplimentelor de vitamina A , vitaminele B , vitamina D sau vitamina E nu reduce riscul de cancer pulmonar. Suplimentarea cu vitamina C ar putea reduce riscul de cancer pulmonar. Unele studii au descoperit că vitaminele A, B și E pot crește riscul de cancer pulmonar la cei care au un istoric de fumat.
Unele studii sugerează că persoanele care mănâncă alimente cu o proporție mai mare de legume și fructe tind să aibă un risc mai mic, dar acest lucru se poate datora confuziei - riscul mai scăzut, de fapt, datorită asocierii unei diete bogate în fructe și legume cu mai puțin fumat. . Mai multe studii riguroase nu au demonstrat o asociere clară între dietă și riscul de cancer pulmonar, deși meta-analiză care ține cont de starea de fumat poate arăta beneficii de pe urma unei diete sănătoase.
management
Tratamentul pentru cancerul pulmonar depinde de tipul de celule specifice cancerului, de cât de departe s-a răspândit și de starea de performanță a persoanei . Tratamentele comune includ îngrijire paliativă , chirurgie , chimioterapie și radioterapie . Terapia țintită a cancerului pulmonar este din ce în ce mai importantă pentru cancerul pulmonar avansat. În plus, uneori se recomandă renunțarea la fumat și exercițiile fizice.
Interventie chirurgicala

Dacă investigațiile confirmă NSCLC, stadiul este evaluat pentru a determina dacă boala este localizată și supusă intervenției chirurgicale sau dacă s-a răspândit până la punctul în care nu poate fi vindecată chirurgical. Scanarea CT și PET-CT, teste neinvazive, pot fi utilizate pentru a ajuta la excluderea malignității sau a implicării ganglionilor mediastinali . Dacă se suspectează implicarea ganglionilor mediastinali folosind PET-CT, ganglionii pot fi prelevați (folosind o biopsie) pentru a asista stadializarea, o scanare PET-CT nu este suficient de precisă pentru a fi utilizată singură. Tehnicile utilizate pentru obținerea unei probe includ aspirația transtoracică cu ac , aspirația transbronșică cu ac (cu sau fără ecografie endobronșică ), ecografie endoscopică cu aspirație cu ac, mediastinoscopia și toracoscopie . Testele de sânge și testarea funcției pulmonare sunt folosite pentru a evalua dacă o persoană este suficient de bine pentru o intervenție chirurgicală. Dacă testele funcției pulmonare evidențiază o rezervă respiratorie scăzută, este posibil ca intervenția chirurgicală să nu fie posibilă.
În majoritatea cazurilor de NSCLC în stadiu incipient, îndepărtarea unui lob pulmonar ( lobectomie ) este tratamentul chirurgical de elecție. La persoanele care nu sunt apte pentru o lobectomie completă, poate fi efectuată o excizie sublobară mai mică ( rezecție cu pană ). Cu toate acestea, rezecția în pană are un risc mai mare de recidivă decât lobectomia. Brahiterapia cu iod radioactiv la marginile exciziei pene poate reduce riscul de recidivă. Rareori, se efectuează îndepărtarea unui plămân întreg ( pneumonectomie ). Chirurgia toracoscopică video-asistată (VATS) și lobectomia VATS utilizează o abordare minim invazivă a chirurgiei cancerului pulmonar. Lobectomia VATS este la fel de eficientă în comparație cu lobectomia deschisă convențională, cu mai puține boli postoperatorii.
În SCLC, se utilizează de obicei chimioterapia sau radioterapia, sau uneori ambele. Cu toate acestea, rolul intervenției chirurgicale în SCLC este reconsiderat. Chirurgia ar putea îmbunătăți rezultatele atunci când este adăugată chimioterapiei și radiațiilor în SCLC în stadiu incipient.
Eficacitatea chirurgiei (rezecției) cancerului pulmonar pentru persoanele cu NSCLC în stadiul I – IIA nu este clară, dar dovezi slabe sugerează că o abordare combinată a rezecției cancerului pulmonar și îndepărtarea ganglionilor limfatici mediastinali (disecția ganglionilor mediastinali) poate îmbunătăți supraviețuirea în comparație cu rezecție pulmonară și o probă de ganglioni mediastinali (nu o disecție completă a ganglionilor).
Radioterapie

Radioterapia este adesea administrată împreună cu chimioterapia și poate fi utilizată cu intenție curativă la persoanele cu NSCLC care nu sunt eligibile pentru intervenție chirurgicală. Această formă de radioterapie de mare intensitate se numește radioterapie radicală. O perfecționare a acestei tehnici este radioterapia continuă hiperfracționată accelerată (CHART), în care se administrează o doză mare de radioterapie într-o perioadă scurtă de timp. Radiochirurgia se referă la tehnica de radioterapie prin care se administrează o doză mare precisă de radioterapie, care este ghidată de un computer. Radioterapia toracică postoperatorie ( adjuvantă ), în general, nu este utilizată după o intervenție chirurgicală cu intenție curativă pentru NSCLC. Unele persoane cu afectare a ganglionilor limfatici mediastinali N2 ar putea beneficia de radioterapie postoperatorie.
Pentru cazurile de SCLC potențial curabile tratate chirurgical, se recomandă radioterapia toracică postoperatorie. Momentul ideal al acestor terapii (momentul optim pentru administrarea radioterapiei și chimioterapiei pentru îmbunătățirea supraviețuirii) nu este cunoscut.
Dacă creșterea cancerului blochează o secțiune scurtă a bronhiilor, brahiterapia (radioterapia localizată) poate fi administrată direct în interiorul căilor respiratorii pentru a deschide pasajul. În comparație cu radioterapia cu fascicul extern , brahiterapia permite o reducere a timpului de tratament și o expunere redusă la radiații pentru personalul medical. Cu toate acestea, dovezile pentru brahiterapie sunt mai puține decât cele pentru radioterapie cu fascicul extern.
Iradierea profilactică craniană este un tip de radioterapie la creier, utilizat pentru a reduce riscul de metastază. PCI este utilizat în SCLC. În boala în stadiu limitat, PCI crește supraviețuirea la trei ani de la 15% la 20%; în boala extinsă, supraviețuirea la un an crește de la 13% la 27%. Pentru persoanele care au NSCLC și o singură metastază cerebrală, nu este clar dacă intervenția chirurgicală este mai eficientă decât radiochirurgia.
Îmbunătățirile recente în direcționarea și imagistica au condus la dezvoltarea radiațiilor stereotactice în tratamentul cancerului pulmonar în stadiu incipient. În această formă de radioterapie, dozele mari sunt eliberate pe parcursul unui număr de sesiuni folosind tehnici de țintire stereotactică. Utilizarea sa este în primul rând la pacienții care nu sunt candidați la intervenții chirurgicale din cauza comorbidităților medicale .
Atât pentru pacienții cu NSCLC, cât și pentru cei cu SCLC, pot fi utilizate doze mai mici de radiații în piept pentru controlul simptomelor ( radioterapia paliativă ). Nu s-a demonstrat că utilizarea dozelor mai mari de radioterapie pentru îngrijiri paliative prelungește supraviețuirea.
Chimioterapia
Regimul de chimioterapie depinde de tipul tumorii. SCLC, chiar și boala în stadiu relativ incipient, este tratată în primul rând cu chimioterapie și radiații. În SCLC, cisplatina și etoposida sunt cele mai frecvent utilizate. Sunt de asemenea utilizate combinații cu carboplatină , gemcitabină , paclitaxel , vinorelbină , topotecan și irinotecan . În NSCLC avansat, chimioterapia îmbunătățește supraviețuirea și este utilizată ca tratament de primă linie, cu condiția ca persoana să fie suficient de bine pentru tratament. De obicei, se folosesc două medicamente, dintre care unul este adesea pe bază de platină (fie cisplatină, fie carboplatină). Alte medicamente utilizate frecvent sunt gemcitabina, paclitaxelul, docetaxelul , pemetrexedul , etoposida sau vinorelbina. Medicamentele pe bază de platină și combinațiile care includ terapia cu platină nu par a fi mai benefice pentru prelungirea supraviețuirii în comparație cu alte medicamente care nu sunt cu platină și pot duce la un risc mai mare de reacții adverse grave, cum ar fi greață, vărsături, anemie și trombocitopenie, în special la persoanele cu vârsta peste 70 de ani. Dovezile sunt insuficiente pentru a determina care abordare chimioterapie este asociată cu cea mai înaltă calitate a vieții. De asemenea, lipsesc dovezi pentru a determina dacă tratarea persoanelor cu NSCLC a doua oară atunci când prima rundă de chimioterapie nu a avut succes (chimioterapia de linia a doua) provoacă mai mult beneficiu sau rău.
Chimioterapia adjuvantă se referă la utilizarea chimioterapiei după o intervenție chirurgicală aparent curativă pentru a îmbunătăți rezultatul. În NSCLC, sunt prelevate mostre din ganglionii limfatici din apropiere în timpul intervenției chirurgicale pentru a ajuta stadializarea. Dacă boala în stadiul II sau III este confirmată, chimioterapia adjuvantă (inclusiv sau fără radioterapia postoperatorie) îmbunătățește supraviețuirea cu 4% la cinci ani. Combinația de vinorelbină și cisplatină este mai eficientă decât regimurile mai vechi. Chimioterapia adjuvantă pentru persoanele cu cancer în stadiul IB este controversată, deoarece studiile clinice nu au demonstrat în mod clar un beneficiu de supraviețuire. Chimioterapia înainte de intervenția chirurgicală în NSCLC, care poate fi îndepărtată chirurgical, poate îmbunătăți rezultatele.
Chimioterapia poate fi combinată cu îngrijirea paliativă în tratamentul NSCLC. În cazurile avansate, chimioterapia adecvată îmbunătățește supraviețuirea medie decât îngrijirea de susținere, precum și îmbunătățirea calității vieții . Cu o condiție fizică adecvată , menținerea chimioterapiei în timpul paliației cancerului pulmonar oferă 1,5 până la 3 luni de prelungire a supraviețuirii, ameliorarea simptomatică și o îmbunătățire a calității vieții, cu rezultate mai bune observate cu agenții moderni. NSCLC Meta-Analyses Collaborative Group recomandă dacă beneficiarul dorește și poate tolera tratamentul, atunci chimioterapia poate fi luată în considerare în NSCLC avansat.
Dirijată și imunoterapie
Sunt disponibile mai multe medicamente care vizează căile moleculare în cancerul pulmonar, în special pentru tratamentul bolilor avansate. Erlotinib , gefitinib și afatinib inhibă tirozin kinaza la nivelul receptorului factorului de creștere epidermic (EGFR). Acești inhibitori EGFR pot ajuta la întârzierea răspândirii celulelor canceroase pentru persoanele cu cancer pulmonar EGFR M+ și pot îmbunătăți calitatea vieții unei persoane. Nu s-a demonstrat că inhibitorii EGFR ajută oamenii să supraviețuiască mai mult. Pentru persoanele cu mutații EGFR, tratamentul cu gefitinib poate duce la o îmbunătățire a calității vieții în comparație cu tratamentul cu chimioterapie. Denosumab , un anticorp monoclonal îndreptat împotriva activatorului receptorului ligandului factorului nuclear kappa-B , poate fi util în tratamentul metastazelor osoase .

Imunoterapia poate fi utilizată atât pentru SCLC, cât și pentru NSCLC. Celulele NSCLC care exprimă ligandul de moarte programată 1 (PD-L1) ar putea interacționa cu receptorul de moarte programată 1 (PD-1) exprimat pe suprafața celulelor T și poate duce la o scădere a uciderii celulelor tumorale de către sistemul imunitar. Atezolizumab este un anticorp monoclonal anti PD-L1. Nivolumab și Pembrolizumab sunt anticorpi monoclonali anti PD-1. Ipilimumab este un anticorp monoclonal care vizează proteina 4 asociată limfocitelor T citotoxice (CTLA-4) de pe suprafața celulelor T. Bevacizumab este un anticorp monoclonal care vizează factorul de creștere a endoteliului vascular în circulație și funcționează ca un inhibitor al angiogenezei. Au fost publicate mai multe studii clinice de fază 3 care utilizează imunoterapia în prima linie pentru tratamentul NSCLC, inclusiv Pembrolizumab în KEYNOTE-024, KEYNOTE-042, KEYNOTE-189 și KEYNOTE-407; Nivolumab și Ipilimumab în CHECKMATE-227 și CHECKMATE 9LA; și Atezolizumab în IMpower110, IMpower130 și IMpower150.

Tratamentul cu imunoterapie pe bază de vaccin după operație sau radioterapie poate să nu conducă la o supraviețuire îmbunătățită pentru persoanele cu NSCLC în stadiile I-III.
Bronhoscopie
Mai multe tratamente pot fi furnizate prin bronhoscopie pentru managementul obstrucției sau sângerării căilor aeriene. Dacă o cale respiratorie devine obstrucționată de creșterea cancerului, opțiunile includ bronhoscopia rigidă, bronhoplastia cu balon, stentarea și microdebridarea. Fotosecția cu laser implică livrarea luminii laser în interiorul căilor respiratorii prin intermediul unui bronhoscop pentru a îndepărta tumora obstructivă.
Îngrijire paliativă
Îngrijirea paliativă, atunci când este adăugată la îngrijirea obișnuită a cancerului, aduce beneficii oamenilor chiar și atunci când aceștia încă primesc chimioterapie. Aceste abordări permit discuții suplimentare despre opțiunile de tratament și oferă oportunități de a ajunge la decizii bine gândite. Îngrijirea paliativă poate evita îngrijirea inutilă, dar costisitoare, nu numai la sfârșitul vieții, ci și pe tot parcursul bolii. Pentru persoanele care au o boală mai avansată, îngrijirea hospice poate fi, de asemenea, adecvată.
Intervenții neinvazive
Cea mai eficientă intervenție pentru evitarea decesului din cauza cancerului pulmonar este renunțarea la fumat; chiar și persoanele care au deja cancer pulmonar sunt încurajate să renunțe la fumat. Nu există dovezi clare care programul de renunțare la fumat este cel mai eficient pentru persoanele care au fost diagnosticate cu cancer pulmonar.
Unele dovezi slabe sugerează că anumite intervenții de îngrijire de susținere ( noninvazive ) care se concentrează pe bunăstarea persoanelor cu cancer pulmonar pot îmbunătăți calitatea vieții. Intervenții precum urmărirea asistentelor medicale, psihoterapia , terapia psihosocială și programele educaționale pot fi benefice, cu toate acestea, dovezile nu sunt puternice (sunt necesare cercetări suplimentare). Consilierea poate ajuta oamenii să facă față simptomelor emoționale legate de cancerul pulmonar. Reflexologia poate fi eficientă pe termen scurt, totuși este nevoie de mai multe cercetări. Nu s-au găsit dovezi care să sugereze că intervențiile nutriționale sau programele de exerciții fizice pentru o persoană cu cancer pulmonar au ca rezultat o îmbunătățire a calității vieții care sunt relevante sau durează foarte mult.
Antrenamentele pot beneficia de persoanele cu NSCLC care se recuperează după o intervenție chirurgicală pulmonară. În plus, antrenamentul poate beneficia de persoanele cu NSCLC care au primit radioterapie, chimioterapie, chimioradioterapie sau îngrijiri paliative. Antrenamentul fizic înainte de operația de cancer pulmonar poate îmbunătăți, de asemenea, rezultatele. Nu este clar dacă antrenamentul sau programele de exerciții sunt benefice pentru persoanele care au cancer pulmonar în stadiu avansat. O componentă la domiciliu într-un program personalizat de reabilitare fizică poate fi utilă pentru recuperare. Nu este clar dacă preabilitarea la domiciliu (înainte de operație) duce la mai puține evenimente adverse sau timp de spitalizare. Reabilitarea fizică cu o componentă la domiciliu poate îmbunătăți recuperarea după tratament și sănătatea generală a plămânilor.
Prognoză
| Stadiul clinic | Supraviețuire la cinci ani (%) | |
|---|---|---|
| Carcinom pulmonar fără celule mici | Carcinom pulmonar cu celule mici | |
| in absenta | 50 | 38 |
| IB | 47 | 21 |
| IIA | 36 | 38 |
| IIB | 26 | 18 |
| IIIA | 19 | 13 |
| IIIB | 7 | 9 |
| IV | 2 | 1 |
Dintre toți oamenii cu cancer pulmonar din SUA, aproximativ 17% până la 20% supraviețuiesc cel puțin cinci ani după diagnostic. În Anglia și Țara Galilor, între 2013 și 2017, supraviețuirea totală de cinci ani pentru cancerul pulmonar a fost estimată la 13,8%. Rezultatele sunt în general mai rele în lumea în curs de dezvoltare . Din cauza depistarii tardive, stadiul cancerului pulmonar este adesea avansat la momentul diagnosticului. La prezentare, aproximativ o treime din cazurile de NSCLC au boală metastatică, iar 60-70% dintre SCLC au boală în stadiu extins. Supraviețuirea pentru cancerul pulmonar scade pe măsură ce stadiul diagnosticului devine mai avansat; datele engleze sugerează că aproximativ 70% dintre pacienți supraviețuiesc cel puțin un an când sunt diagnosticați în stadiul cel mai incipient, dar acest lucru scade la doar 14% pentru cei diagnosticați cu cea mai avansată boală (stadiul IV).
Factorii de prognostic în NSCLC includ prezența simptomelor pulmonare, dimensiunea mare a tumorii (>3 cm), tipul de celule nesquamoase (histologie), gradul de răspândire (stadiul) și metastazele la ganglioni limfatici multipli și invazia vasculară . Pentru persoanele cu boală inoperabilă, rezultatele sunt mai rele la cei cu performanță slabă și pierdere în greutate de peste 10%. Factorii de prognostic în cancerul pulmonar cu celule mici includ starea de performanță, sexul biologic, stadiul bolii și implicarea sistemului nervos central sau a ficatului la momentul diagnosticului.
Pentru NSCLC, cel mai bun prognostic se realizează cu rezecția chirurgicală completă a bolii în stadiul IA, cu până la 70% supraviețuire la cinci ani. Persoanele cu SCLC în stadiu extins au o rată medie de supraviețuire pe cinci ani mai mică de 1%. Timpul mediu de supraviețuire pentru boala în stadiu limitat este de 20 de luni, cu o rată de supraviețuire la cinci ani de 20%. Prognosticul pacienților cu NSCLC sa îmbunătățit semnificativ în ultimii ani odată cu introducerea imunoterapiei. Pacienții cu tumora PDL-1 exprimată peste jumătate sau mai multe dintre celulele tumorale au obținut o supraviețuire globală mediană de 30 de luni cu pembrolizumab. Au fost publicate mai multe studii de fază 3 care oferă imunoterapie în primă linie pentru pacienții cu cancer pulmonar fără celule mici.
Potrivit datelor furnizate de Institutul Național al Cancerului , vârsta medie la momentul diagnosticării cancerului pulmonar în SUA este de 70 de ani, iar vârsta medie la deces este de 72 de ani. În SUA, persoanele cu asigurare medicală au mai multe șanse de a avea un rezultat mai bun.
Epidemiologie
La nivel mondial, cancerul pulmonar este cel mai frecvent cancer la bărbați atât pentru incidență , cât și pentru mortalitate , iar în rândul femeilor are a treia cea mai mare incidență (după cancerul de sân și cancerul colorectal ) și a doua cea mai mare mortalitate (după cancerul de sân). În 2020, în întreaga lume au fost găsite 2,2 milioane de cazuri noi, iar 1,8 milioane de decese s-au datorat cancerului pulmonar, reprezentând 18,0% din totalul deceselor cauzate de cancer. Cele mai mari rate sunt în Micronezia, Polinezia, Europa, Asia, America de Nord și Europa. Ratele din Africa și America Centrală sunt mult mai mici.
Persoanele care au o istorie lungă de fumat au cel mai mare risc de a dezvolta cancer pulmonar, riscul crescând odată cu durata fumatului. Incidența la bărbați a crescut până la mijlocul anilor 1980 și a scăzut de atunci. La femei, incidența a crescut până la sfârșitul anilor 1990 și de atunci a fost stabilă.
La fiecare 3-4 milioane de țigări fumate, poate apărea un deces prin cancer pulmonar. Influența „ Big Tobacco ” joacă un rol semnificativ în fumat. Tinerii nefumători care văd reclame la tutun sunt mai predispuși să fumeze. Rolul fumatului pasiv este din ce în ce mai recunoscut ca un factor de risc pentru cancerul pulmonar, rezultând intervenții politice pentru a reduce expunerea nedorită a nefumătorilor la fumul de tutun al altora.
Din anii 1960, ratele adenocarcinomului pulmonar au început să crească în raport cu alte tipuri de cancer pulmonar, parțial datorită introducerii țigărilor cu filtru. Utilizarea filtrelor elimină particulele mai mari din fumul de tutun, reducând astfel depunerea în căile respiratorii mai mari. Cu toate acestea, fumătorul trebuie să inspire mai profund pentru a primi aceeași cantitate de nicotină , crescând depunerea de particule în căile respiratorii mici, unde tinde să apară adenocarcinomul. Ratele de adenocarcinom pulmonar continuă să crească.
Statele Unite
În SUA, atât bărbații de culoare, cât și femeile de culoare au o incidență mai mare. Riscul pe parcursul vieții de a dezvolta cancer pulmonar este de 8% la bărbați și de 6% la femei.
De asemenea, în SUA, veteranii militari au o rată de cancer pulmonar cu 25-50% mai mare, în principal din cauza ratelor mai mari de fumat. În timpul celui de-al Doilea Război Mondial și al Războiului din Coreea , azbestul a jucat și el un rol, iar agentul Orange ar fi putut cauza unele probleme în timpul războiului din Vietnam .
Regatul Unit
Cancerul pulmonar este al treilea cel mai frecvent cancer din Marea Britanie (47.968 de persoane au fost diagnosticate cu boala în 2017) și este cea mai frecventă cauză de deces cauzat de cancer (aproximativ 34.600 de persoane au murit în 2018).
Alte țări
Ratele cancerului pulmonar sunt în prezent mai scăzute în țările în curs de dezvoltare. Odată cu creșterea fumatului în țările în curs de dezvoltare, este de așteptat ca ratele să crească în următorii câțiva ani, în special atât în China, cât și în India.
Istorie
Cancerul pulmonar era mai puțin frecvent înainte de apariția fumatului; nici măcar nu a fost recunoscută ca o boală distinctă până în 1761. Diferite aspecte ale cancerului pulmonar au fost descrise în continuare în 1810. Tumorile pulmonare maligne reprezentau doar 1% din toate tipurile de cancer observate la autopsie în 1878, dar crescuseră la 10-15% de către începutul anilor 1900. Rapoartele de cazuri din literatura medicală numărau doar 374 în întreaga lume în 1912, dar o analiză a autopsiilor a arătat că incidența cancerului pulmonar a crescut de la 0,3% în 1852 la 5,66% în 1952. În Germania , în 1929, medicul Fritz Lickint a recunoscut legătura dintre fumat. și cancerul pulmonar, care a dus la o campanie agresivă împotriva fumatului . British Doctors' Study , publicat în anii 1950, a fost prima dovadă epidemiologică solidă a legăturii dintre cancerul pulmonar și fumat. Drept urmare, în 1964, chirurgul general al Statelor Unite a recomandat fumătorilor să renunțe la fumat.
Legătura cu gazul radon a fost recunoscută pentru prima dată în rândul minerilor din Munții Metalici de lângă Schneeberg, Saxonia . Acolo a fost extras argint din 1470, iar aceste mine sunt bogate în uraniu, cu radiu și radon însoțitori. Minerii au dezvoltat o cantitate disproporționată de boli pulmonare, recunoscute în cele din urmă drept cancer pulmonar în anii 1870. În ciuda acestei descoperiri, mineritul a continuat până în anii 1950, din cauza cererii de uraniu a URSS . Radonul a fost confirmat ca o cauză a cancerului pulmonar în anii 1960.
Prima pneumonectomie cu succes pentru cancerul pulmonar a fost efectuată în 1933. Radioterapia paliativă a fost folosită încă din anii 1940. Radioterapia radicală, utilizată inițial în anii 1950, a fost o încercare de a folosi doze mai mari de radiații la pacienții cu cancer pulmonar în stadiu relativ incipient, dar care altfel nu erau apți pentru operație. În 1997, CHART a fost văzut ca o îmbunătățire față de radioterapia radicală convențională. Cu SCLC, încercările inițiale din anii 1960 de rezecție chirurgicală și radioterapia radicală au fost fără succes. În anii 1970, au fost dezvoltate scheme de chimioterapie de succes.
Direcții de cercetare
Căutarea de noi opțiuni de tratament continuă. Multe studii clinice care implică radioterapie, intervenții chirurgicale, inhibitori EGFR, inhibitori de microtubuli și imunoterapie sunt în curs de desfășurare.
Direcțiile de cercetare pentru tratamentul cancerului pulmonar includ imunoterapia , care încurajează sistemul imunitar al organismului să atace celulele tumorale, epigenetica și noi combinații de chimioterapie și radioterapie, atât pe cont propriu, cât și împreună. Multe dintre aceste noi tratamente funcționează prin blocarea punctelor de control imunitar , perturbând capacitatea cancerului de a se sustrage sistemului imunitar .
Ipilimumab blochează semnalizarea printr-un receptor de pe celulele T cunoscut sub numele de CTLA-4 , care atenuează sistemul imunitar. A fost aprobat de Administrația SUA pentru Alimente și Medicamente pentru tratamentul melanomului și este în curs de studii clinice atât pentru NSCLC, cât și pentru SCLC.
Alte tratamente de imunoterapie interferează cu legarea proteinei morții celulare programate 1 (PD-1) cu ligandul său PD-1, ligand 1 (PD-L1) și au fost aprobate ca tratamente de primă linie și ulterioare pentru diferite subseturi de cancere pulmonare. . Semnalizarea prin PD-1 inactivează celulele T. Unele celule canceroase par să exploateze acest lucru prin exprimarea PD-L1 pentru a opri celulele T care le-ar putea recunoaște ca o amenințare. Anticorpii monoclonali care vizează atât PD-1, cât și PD-L1, cum ar fi pembrolizumab , nivolumab , atezolizumab și durvalumab , sunt în prezent în studii clinice pentru tratamentul cancerului pulmonar.
Epigenetica este studiul modificărilor moleculare mici – sau „etichete” – care se leagă de ADN și modifică nivelurile de expresie a genelor . Direcționarea acestor etichete cu medicamente poate ucide celulele canceroase. Cercetările în stadiu incipient în NSCLC, folosind medicamente care vizează modificări epigenetice, arată că blocarea a mai mult de una dintre aceste etichete poate ucide celulele canceroase cu mai puține efecte secundare. De asemenea, studiile arată că administrarea acestor medicamente înainte de tratamentul standard poate îmbunătăți eficacitatea acestuia. Sunt în curs de desfășurare studii clinice pentru a evalua cât de bine aceste medicamente ucid celulele canceroase pulmonare la oameni. Mai multe medicamente care vizează mecanismele epigenetice sunt în dezvoltare. Inhibitorii histon deacetilazei în dezvoltare includ acid valproic , vorinostat , belinostat , panobinostat , entinostat și romidepsin . Inhibitorii de ADN metiltransferaza in dezvoltare includ decitabina , azacitidina si hidralazina .
Proiectul TRACERx analizează modul în care se dezvoltă și evoluează NSCLC și cum aceste tumori devin rezistente la tratament. Proiectul va analiza mostre de tumoră de la 850 de persoane cu NSCLC în diferite stadii, inclusiv diagnostic, după primul tratament, post-tratament și recidivă. Studiind mostre în diferite puncte ale dezvoltării tumorii, cercetătorii speră să identifice schimbările care conduc la creșterea tumorii și rezistența la tratament. Rezultatele acestui proiect vor ajuta oamenii de știință și medicii să obțină o mai bună înțelegere a NSCLC și pot duce la dezvoltarea de noi tratamente pentru boală.
Pentru cazurile de cancer pulmonar care dezvoltă rezistență la receptorul factorului de creștere epidermic (EGFR) și la inhibitorii tirozin kinazei limfom kinazei anaplazice (ALK) , noi medicamente sunt în dezvoltare. Inhibitorii EGFR includ erlotinib , gefitinib , afatinib și icotinib (ultimul este disponibil doar în China). O cale alternativă de semnalizare, c-Met , poate fi inhibată de tivantinib și acceptazumab . Noii inhibitori ALK includ crizotinib și ceritinib . Dacă calea MAPK/ERK este implicată, inhibitorul kinazei BRAF dabrafenib și inhibitorul MAPK/MEK trametinib pot fi benefice.
Calea PI3K a fost investigată ca țintă pentru terapia cancerului pulmonar. Cele mai promițătoare strategii pentru țintirea acestei căi par a fi inhibarea selectivă a unuia sau mai multor membri ai PI3K de clasă I și inhibarea co-țintită a acestei căi cu altele, cum ar fi MEK.
Celulele stem ale cancerului pulmonar sunt adesea rezistente la chimioterapie și radioterapie convențională. Acest lucru poate duce la recidive după tratament. Noile abordări vizează markeri de proteine sau glicoproteine care sunt specifici celulelor stem. Astfel de markeri includ CD133 , CD90 , ALDH1A1 , CD44 şi ABCG2 . Căile de semnalizare precum Hedgehog , Wnt și Notch sunt adesea implicate în auto-reînnoirea liniilor de celule stem. Astfel, tratamentele care vizează aceste căi pot ajuta la prevenirea recidivelor.