Farmacologie -Pharmacology
| Farmacologie | |
|---|---|
 Reprezentare schematică a băii de organe utilizată pentru studiul efectului țesuturilor izolate
| |
| ID unic MeSH | D010600 |
Farmacologia este o ramură a medicinei , biologiei și științelor farmaceutice care se ocupă de acțiunea medicamentului sau a medicamentelor , unde un medicament poate fi definit ca orice moleculă artificială, naturală sau endogenă (din interiorul corpului) care exercită un efect biochimic sau fiziologic asupra celulei. , țesut, organ sau organism (uneori cuvântul pharmacon este folosit ca termen pentru a cuprinde aceste specii bioactive endogene și exogene ). Este știința medicamentelor, inclusiv originea, compoziția, farmacocinetica, utilizarea terapeutică și toxicologia acestora. Mai precis, este studiul interacțiunilor care apar între un organism viu și substanțele chimice care afectează funcția biochimică normală sau anormală. Dacă substanțele au proprietăți medicinale, acestea sunt considerate produse farmaceutice .
Domeniul cuprinde compoziția și proprietățile medicamentelor, funcțiile, sursele, sinteza și proiectarea medicamentelor, mecanisme moleculare și celulare , mecanisme de organe/sisteme, transducție a semnalului/comunicare celulară, diagnosticare moleculară , interacțiuni , biologie chimică , terapie și aplicații medicale și capacități antipatogene. Cele două domenii principale ale farmacologiei sunt farmacodinamia și farmacocinetica . Farmacodinamica studiază efectele unui medicament asupra sistemelor biologice, iar farmacocinetica studiază efectele sistemelor biologice asupra unui medicament. În termeni largi, farmacodinamia discută substanțele chimice cu receptorii biologici , iar farmacocinetica discută absorbția , distribuția, metabolismul și excreția (ADME) a substanțelor chimice din sistemele biologice.
Farmacologia nu este sinonimă cu farmacia și cei doi termeni sunt frecvent confundați. Farmacologia, o știință biomedicală , se ocupă cu cercetarea, descoperirea și caracterizarea substanțelor chimice care prezintă efecte biologice și elucidarea funcției celulare și organismelor în legătură cu aceste substanțe chimice. În contrast, farmacia, o profesie de servicii de sănătate, este preocupată de aplicarea principiilor învățate din farmacologie în mediile sale clinice; fie că este vorba de un rol de distribuire sau de îngrijire clinică. În ambele domenii, contrastul principal dintre cele două este distincția dintre îngrijirea directă a pacientului, practica farmaceutică și domeniul de cercetare orientat spre știință, condus de farmacologie.
Etimologie
Cuvântul farmacologie este derivat din greaca φάρμακον , pharmakon , „medicament, otravă ” și -λογία , -logia „studiul”, „cunoașterea” (cf. etimologia farmaciei ) . Pharmakon este legat de pharmakos , sacrificiul ritualic sau exilul unui țap ispășitor uman sau al unei victime în religia greacă antică .
Termenul modern pharmacon este folosit mai larg decât termenul de drog deoarece include substanțe endogene și substanțe biologic active care nu sunt utilizate ca medicamente. De obicei, include agonişti şi antagonişti farmacologici , dar şi inhibitori de enzime (cum ar fi inhibitorii de monoaminooxidază ).
Istorie


Originile farmacologiei clinice datează din Evul Mediu , cu farmacognozie și Canonul medicinei al lui Avicenna , Comentariul lui Petru al Spaniei despre Isaac și Comentariul lui Ioan de Sf. Amand asupra antedotarului lui Nicolae . Farmacologia timpurie s-a concentrat pe plante medicinale și substanțe naturale, în principal extracte de plante. Medicamentele au fost compilate în cărți numite farmacopei . Drogurile brute au fost folosite încă din preistorie ca preparat de substanțe din surse naturale. Cu toate acestea, ingredientul activ al medicamentelor brute nu este purificat și substanța este alterată cu alte substanțe.
Medicina tradițională variază între culturi și poate fi specifică unei anumite culturi, cum ar fi medicina tradițională chineză , mongolă , tibetană și coreeană . Cu toate acestea, o mare parte din aceasta a fost considerată de atunci ca pseudoștiință . Substanțele farmacologice cunoscute sub numele de entheogeni pot avea uz spiritual și religios și context istoric.
În secolul al XVII-lea, medicul englez Nicholas Culpeper a tradus și folosit texte farmacologice. Culpeper a detaliat plantele și condițiile pe care le-ar putea trata. În secolul al XVIII-lea, o mare parte din farmacologia clinică a fost stabilită prin munca lui William Withering . Farmacologia ca disciplină științifică nu a avansat mai mult decât la mijlocul secolului al XIX-lea, pe fondul marii renașteri biomedicale din acea perioadă. Înainte de a doua jumătate a secolului al XIX-lea, potența și specificitatea remarcabile a acțiunilor unor medicamente precum morfina , chinina și digitala erau explicate vag și cu referire la puteri chimice extraordinare și afinități pentru anumite organe sau țesuturi. Prima secție de farmacologie a fost înființată de Rudolf Buchheim în 1847, la Universitatea din Tartu, ca recunoaștere a necesității de a înțelege modul în care medicamentele și otrăvurile și-au produs efectele terapeutice. Ulterior, primul departament de farmacologie din Anglia a fost înființat în 1905 la University College London .
Farmacologia s-a dezvoltat în secolul al XIX-lea ca o știință biomedicală care a aplicat principiile experimentării științifice în contexte terapeutice. Avansarea tehnicilor de cercetare a propulsat cercetarea și înțelegerea farmacologică. Dezvoltarea preparatului băii de organe , în care probele de țesut sunt conectate la dispozitive de înregistrare, cum ar fi un miograf , iar răspunsurile fiziologice sunt înregistrate după aplicarea medicamentului, a permis analiza efectelor medicamentelor asupra țesuturilor. Dezvoltarea testului de legare a ligandului în 1945 a permis cuantificarea afinității de legare a medicamentelor la țintele chimice. Farmacologii moderni folosesc tehnici din genetică , biologie moleculară , biochimie și alte instrumente avansate pentru a transforma informațiile despre mecanismele moleculare și ținte în terapii îndreptate împotriva bolilor, defectelor sau agenților patogeni și creează metode de îngrijire preventivă, diagnosticare și, în cele din urmă, medicină personalizată .
Diviziuni
Disciplina de farmacologie poate fi împărțită în mai multe subdiscipline, fiecare cu un accent specific.
Sistemele corpului

Farmacologia se poate concentra, de asemenea, pe sisteme specifice care cuprind organismul. Diviziunile legate de sistemele corporale studiază efectele medicamentelor în diferite sisteme ale corpului. Acestea includ neurofarmacologia , în sistemul nervos central și periferic ; imunofarmacologie în sistemul imunitar. Alte divizii includ farmacologia cardiovasculară , renală și endocrină . Psihofarmacologia este studiul utilizării medicamentelor care afectează psihicul , mintea și comportamentul (de exemplu, antidepresive) în tratarea tulburărilor mintale (de exemplu, depresia). Acesta încorporează abordări și tehnici din neurofarmacologie, comportamentul animal și neuroștiința comportamentală și este interesat de mecanismele comportamentale și neurobiologice de acțiune ale medicamentelor psihoactive. Domeniul conex al neuropsihofarmacologiei se concentrează pe efectele medicamentelor la suprapunerea dintre sistemul nervos și psihic.
Farmacometabolomica , cunoscută și sub denumirea de farmacometabonomica, este un domeniu care provine din metabolomică , cuantificarea și analiza metaboliților produși de organism. Se referă la măsurarea directă a metaboliților din fluidele corporale ale unui individ, pentru a prezice sau evalua metabolismul compușilor farmaceutici și pentru a înțelege mai bine profilul farmacocinetic al unui medicament. Farmacometabolomica poate fi aplicată pentru a măsura nivelurile metaboliților în urma administrării unui medicament, pentru a monitoriza efectele medicamentului asupra căilor metabolice. Farmacomicrobiomica studiază efectul variațiilor microbiomului asupra dispoziției, acțiunii și toxicității medicamentelor. Farmacomicrobiomica se ocupă de interacțiunea dintre medicamente și microbiomul intestinal . Farmacogenomica este aplicarea tehnologiilor genomice pentru descoperirea de medicamente și caracterizarea ulterioară a medicamentelor legate de întregul genom al unui organism. Pentru farmacologia genelor individuale, farmacogenetica studiază modul în care variația genetică dă naștere unor răspunsuri diferite la medicamente. Farmacoepigenetica studiază modelele de marcare epigenetică subiacente care duc la variații în răspunsul unui individ la tratamentul medical.
Practica clinică și descoperirea medicamentelor

Farmacologia poate fi aplicată în științele clinice. Farmacologia clinică este aplicarea metodelor și principiilor farmacologice în studiul medicamentelor la om. Un exemplu în acest sens este posologia, care este studiul modului în care sunt dozate medicamentele.
Farmacologia este strâns legată de toxicologie . Atât farmacologia, cât și toxicologia sunt discipline științifice care se concentrează pe înțelegerea proprietăților și acțiunilor substanțelor chimice. Cu toate acestea, farmacologia subliniază efectele terapeutice ale substanțelor chimice, de obicei medicamente sau compuși care ar putea deveni medicamente, în timp ce toxicologia este studiul efectelor adverse ale substanțelor chimice și evaluarea riscurilor.
Cunoștințele farmacologice sunt folosite pentru a consilia farmacoterapie în medicină și farmacie .
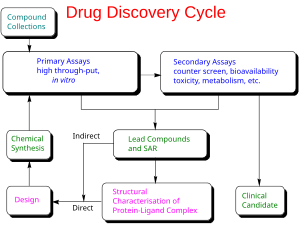
Descoperirea drogului
Descoperirea medicamentelor este domeniul de studiu preocupat de crearea de noi medicamente. Acesta cuprinde subdomeniile proiectării și dezvoltării medicamentelor . Descoperirea medicamentelor începe cu proiectarea medicamentelor, care este procesul inventiv de găsire de noi medicamente. În sensul cel mai elementar, aceasta implică proiectarea de molecule care sunt complementare ca formă și încărcare unei ținte biomoleculare date. După ce un compus plumb a fost identificat prin descoperirea unui medicament, dezvoltarea medicamentului implică aducerea medicamentului pe piață. Descoperirea medicamentelor este legată de farmacoeconomia , care este subdisciplina economiei sănătății care ia în considerare valoarea medicamentelor. Farmacoeconomia evaluează costurile și beneficiile medicamentelor pentru a ghida alocarea optimă a resurselor medicale. Tehnicile utilizate pentru descoperirea , formularea , fabricarea și controlul calității descoperirii medicamentelor sunt studiate de ingineria farmaceutică , o ramură a ingineriei . Farmacologia de siguranță este specializată în detectarea și investigarea potențialelor efecte nedorite ale medicamentelor.
|
|
Dezvoltarea medicamentelor este o preocupare vitală pentru medicină , dar are și implicații economice și politice puternice . Pentru a proteja consumatorul și a preveni abuzul, multe guverne reglementează fabricarea, vânzarea și administrarea medicamentelor. În Statele Unite , principalul organism care reglementează produsele farmaceutice este Food and Drug Administration ; pun în aplicare standardele stabilite de Farmacopeea Statelor Unite . În Uniunea Europeană , principalul organism care reglementează produsele farmaceutice este EMA , care aplică standardele stabilite de Farmacopeea Europeană .
Stabilitatea metabolică și reactivitatea unei biblioteci de compuși de medicamente candidați trebuie evaluate pentru metabolizarea medicamentelor și studii toxicologice. Au fost propuse multe metode pentru predicțiile cantitative în metabolismul medicamentelor; un exemplu de metodă de calcul recentă este SPORCalc. O ușoară modificare a structurii chimice a unui compus medicinal i-ar putea modifica proprietățile medicinale, în funcție de modul în care modificarea se raportează la structura substratului sau a situsului receptor asupra căruia acționează: aceasta se numește relație de activitate structurală (SAR). Când a fost identificată o activitate utilă, chimiștii vor produce mulți compuși similari numiți analogi, pentru a încerca să maximizeze efectul (efectele) medicinal(e) dorit(e). Acest lucru poate dura de la câțiva ani până la un deceniu sau mai mult și este foarte costisitor. De asemenea, trebuie să se stabilească cât de sigur este consumat medicamentul, stabilitatea acestuia în corpul uman și cea mai bună formă de administrare la sistemul de organe dorit, cum ar fi tableta sau aerosolul. După teste ample, care pot dura până la șase ani, noul medicament este gata pentru comercializare și vânzare.
Din cauza acestor intervale de timp lungi și pentru că din fiecare 5000 de medicamente noi potențiale, de obicei, doar unul va ajunge vreodată pe piața liberă, acesta este un mod costisitor de a face lucrurile, care costă adesea peste 1 miliard de dolari. Pentru a recupera această cheltuială, companiile farmaceutice pot face o serie de lucruri:
- Investigați cu atenție cererea pentru noul lor produs potențial înainte de a cheltui o cheltuială din fondurile companiei.
- Obțineți un brevet pentru noul medicament, împiedicând alte companii să producă acel medicament pentru o anumită alocare de timp.
Legea inversă a beneficiului descrie relația dintre beneficiile terapeutice ale unui medicament și comercializarea acestuia.
La proiectarea medicamentelor, efectul placebo trebuie luat în considerare pentru a evalua adevărata valoare terapeutică a medicamentului.
Dezvoltarea medicamentelor folosește tehnici de la chimia medicinală până la proiectarea chimică a medicamentelor. Acest lucru se suprapune cu abordarea biologică de a găsi ținte și efecte fiziologice.
Contexte mai largi
Farmacologia poate fi studiată în raport cu contexte mai largi decât fiziologia indivizilor. De exemplu, farmacoepidemiologia se referă la variațiile efectelor medicamentelor în sau între populații, este puntea dintre farmacologia clinică și epidemiologie . Farmacomediul sau farmacologia de mediu este studiul efectelor produselor farmaceutice utilizate și ale produselor de îngrijire personală (PPCP) asupra mediului după eliminarea lor din organism. Sănătatea umană și ecologia sunt strâns legate, astfel încât farmacologia de mediu studiază efectul asupra mediului al medicamentelor și produselor farmaceutice și al produselor de îngrijire personală în mediu .
Drogurile pot avea și importanță etnoculturală, astfel încât etnofarmacologia studiază aspectele etnice și culturale ale farmacologiei.
Câmpuri emergente
Fotofarmacologia este o abordare emergentă în medicină în care medicamentele sunt activate și dezactivate cu lumină . Energia luminii este folosită pentru a schimba forma și proprietățile chimice ale medicamentului, rezultând o activitate biologică diferită. Acest lucru se face pentru a obține în cele din urmă controlul când și unde medicamentele sunt active într-o manieră reversibilă, pentru a preveni efectele secundare și poluarea medicamentelor în mediu.
Teoria farmacologiei

Studiul substanțelor chimice necesită o cunoaștere intimă a sistemului biologic afectat. Odată cu creșterea cunoștințelor de biologie celulară și biochimie , și domeniul farmacologiei s-a schimbat substanțial. A devenit posibil, prin analiza moleculară a receptorilor , să se proiecteze substanțe chimice care acționează asupra semnalizării celulare specifice sau a căilor metabolice prin afectarea site-urilor direct pe receptorii de suprafață celulară (care modulează și mediază căile de semnalizare celulară care controlează funcția celulară).
Substanțele chimice pot avea proprietăți și efecte farmacologic relevante. Farmacocinetica descrie efectul organismului asupra substanței chimice (de exemplu, timpul de înjumătățire și volumul de distribuție ), iar farmacodinamia descrie efectul substanței chimice asupra organismului (dorit sau toxic ).
Sisteme, receptori și liganzi
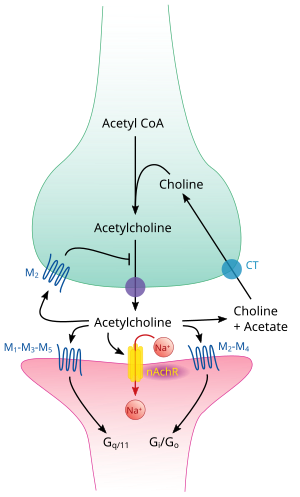
Farmacologia este studiată în mod obișnuit cu privire la anumite sisteme, de exemplu sistemele de neurotransmițători endogeni . Sistemele majore studiate în farmacologie pot fi clasificate după liganzii lor și includ acetilcolina , adrenalină , glutamat , GABA , dopamină , histamina , serotonina , canabinoizi și opioizi .
Țintele moleculare în farmacologie includ receptorii , enzimele și proteinele de transport membranar . Enzimele pot fi vizate cu inhibitori de enzime . Receptorii sunt de obicei clasificați în funcție de structură și funcție. Tipurile majore de receptori studiate în farmacologie includ receptorii cuplați cu proteina G , canalele ionice cu funcție de ligand și receptorii tirozin kinaze .
Farmacodinamica
Farmacodinamica este definită ca modul în care organismul reacționează la medicamente. Modelele farmacologice includ ecuația Hill , ecuația Cheng-Prusoff și regresia Schild . Teoria farmacodinamicii investighează adesea afinitatea de legare a liganzilor de receptorii lor.
Se spune că medicamentul are un indice terapeutic îngust sau larg , un anumit factor de siguranță sau o fereastră terapeutică . Acesta descrie raportul dintre efectul dorit și efectul toxic. Un compus cu un indice terapeutic îngust (aproape de unu) își exercită efectul dorit la o doză apropiată de doza sa toxică. Un compus cu un indice terapeutic larg (mai mare de cinci) își exercită efectul dorit la o doză substanțial sub doza sa toxică. Cei cu o marjă îngustă sunt mai dificil de dozat și administrat și pot necesita monitorizarea medicamentelor terapeutice (exemple sunt warfarina , unele antiepileptice , antibioticele aminoglicozide ). Majoritatea medicamentelor anticancer au o marjă terapeutică îngustă: efectele secundare toxice sunt aproape întotdeauna întâlnite la dozele utilizate pentru a ucide tumorile .
Efectul medicamentelor poate fi descris cu aditivitatea Loewe , care este unul dintre modelele de referință comune.
Farmacocinetica
Farmacocinetica este studiul absorbției, distribuției, metabolismului și excreției de către organism a medicamentelor.
Când descriu proprietățile farmacocinetice ale substanței chimice care este ingredientul activ sau ingredientul farmaceutic activ (API), farmacologii sunt adesea interesați de L-ADME :
- Eliberare – Cum este API-ul dezintegrat (pentru formele orale solide (descompunerea în particule mai mici), dispersat sau dizolvat din medicament?
- Absorbție – Cum este absorbit API (prin piele , intestin , mucoasa bucală )?
- Distribuție – Cum se răspândește API-ul prin organism?
- Metabolism – Este API-ul convertit chimic în interiorul corpului și în ce substanțe. Sunt active (și acestea)? Ar putea fi toxice?
- Excreție – Cum se excretă API (prin bilă, urină, respirație, piele)?
Metabolismul medicamentelor este evaluat în farmacocinetică și este important în cercetarea și prescrierea medicamentelor.
Administrare, politica de droguri si siguranta
Politica drogurilor
În Statele Unite ale Americii , Administrația pentru Alimente și Medicamente (FDA) este responsabilă pentru crearea liniilor directoare pentru aprobarea și utilizarea medicamentelor. FDA cere ca toate medicamentele aprobate să îndeplinească două cerințe:
- Medicamentul trebuie dovedit a fi eficient împotriva bolii pentru care se solicită aprobarea (unde „eficient” înseamnă doar că medicamentul a avut rezultate mai bune decât placebo sau concurenții în cel puțin două studii).
- Medicamentul trebuie să îndeplinească criteriile de siguranță, fiind supus testării animale și controlate pe oameni.
Obținerea aprobării FDA durează de obicei câțiva ani. Testele efectuate pe animale trebuie să fie extinse și trebuie să includă mai multe specii pentru a ajuta atât la evaluarea eficacității, cât și a toxicității medicamentului. Doza oricărui medicament aprobat pentru utilizare este destinată să se încadreze într-un interval în care medicamentul produce un efect terapeutic sau rezultatul dorit.
Siguranța și eficacitatea medicamentelor eliberate pe bază de rețetă în SUA sunt reglementate de Legea federală de comercializare a medicamentelor din 1987 .
Agenția de reglementare a medicamentelor și a produselor de îngrijire medicală (MHRA) are un rol similar în Marea Britanie.
Medicare Part D este un plan de medicamente eliberate pe bază de rețetă în SUA
Prescription Drug Marketing Act (PDMA) este un act legat de politica privind medicamentele.
Medicamentele eliberate pe bază de rețetă sunt medicamente reglementate de legislație.
Societăți și educație
Societăți și administrație
Uniunea Internațională de Farmacologie de bază și clinică , Federația Societăților Europene de Farmacologie și Asociația Europeană pentru Farmacologie Clinică și Terapeutică sunt organizații care reprezintă standardizarea și reglementarea farmacologiei clinice și științifice.
Au fost dezvoltate sisteme de clasificare medicală a medicamentelor cu coduri farmaceutice . Acestea includ Codul Național al Medicamentului (NDC), administrat de Food and Drug Administration .; Numărul de identificare a medicamentelor (DIN), administrat de Health Canada în conformitate cu Legea privind alimentele și medicamentele ; Înregistrarea medicamentelor din Hong Kong , administrată de Serviciul Farmaceutic al Departamentului de Sănătate (Hong Kong) și Indexul Național al Produselor Farmaceutice din Africa de Sud. Au fost dezvoltate, de asemenea, sisteme ierarhice, inclusiv Sistemul de Clasificare Anatomical Therapeutic Chemical (AT, sau ATC/DDD), administrat de Organizația Mondială a Sănătății ; Generic Product Identifier (GPI), un număr de clasificare ierarhic publicat de MediSpan și SNOMED , axa C. Ingredientele medicamentelor au fost clasificate în funcție de identificatorul unic de ingrediente .
Educaţie
Studiul farmacologiei se suprapune cu științele biomedicale și este studiul efectelor medicamentelor asupra organismelor vii. Cercetarea farmacologică poate duce la noi descoperiri de medicamente și poate promova o mai bună înțelegere a fiziologiei umane . Studenții de farmacologie trebuie să aibă cunoștințe de lucru detaliate ale aspectelor din fiziologie, patologie și chimie. Ele pot necesita, de asemenea, cunoașterea plantelor ca surse de compuși activi din punct de vedere farmacologic. Farmacologia modernă este interdisciplinară și implică științe biofizice și computaționale și chimie analitică. Un farmacist trebuie să fie bine echipat cu cunoștințe de farmacologie pentru aplicare în cercetarea farmaceutică sau în practica farmaceutică în spitale sau organizații comerciale care vând clienților. Farmacologii, totuși, lucrează de obicei într-un laborator care efectuează cercetări sau dezvoltarea de noi produse. Cercetarea farmacologică este importantă în cercetarea academică (medicală și non-medicală), poziții industriale private, scriere științifică, brevete științifice și drept, consultanță, angajare în domeniul biotehnologiei și farmaceutice, industria alcoolului, industria alimentară, criminalistică/aplicarea legii, sănătatea publică și științe de mediu/ecologice. Farmacologia este adesea predată studenților la farmacie și medicină ca parte a curriculum-ului școlii de medicină .
Vezi si
Referințe
linkuri externe
- Societatea Americană pentru Farmacologie și Terapie Experimentală
- Societatea Britanică de Farmacologie
- Conferința Internațională de Armonizare
- Farmacopeea SUA
- Uniunea Internațională de Farmacologie de bază și clinică
- Comitetul IUPHAR pentru nomenclatura receptorilor și clasificarea medicamentelor
- Ghid de farmacologie IUPHAR/BPS
Lectură în continuare
- Foreman JC, Johansen T, Gibb AJ (2009). Manual de farmacologie a receptorilor, ediția a doua . CRC Press. ISBN 9781439887578.
- Brunton L (2011). Brunton LL, Chabner B, Knollmann BC (eds.). Goodman and Gilman's The Pharmacological Basis of Therapeutics (12 ed.). New York: McGraw-Hill. ISBN 978-0-07-162442-8.
- Whalen K (2014). Recenzii ilustrate Lippincott: Farmacologie .