Beta-lactam - Beta-lactam
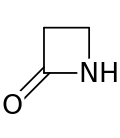
Un inel beta-lactam ( β-lactam ) este un lactam cu patru membri . O lactamă este o amidă ciclică , iar beta- lactamele sunt denumite astfel deoarece atomul de azot este atașat la atomul de β-carbon față de carbonil. Cea mai simplă β-lactamă posibilă este 2-azetidinonă . β-lactamice sunt unități structurale semnificative de medicamente așa cum se manifestă în mai multe antibiotice β-lactam Până la 1970, majoritatea cercetărilor β-lactamic sa preocupat de penicilina și cefalosporina grupuri, dar de atunci, au fost descrise o largă varietate de structuri.
Semnificația clinică
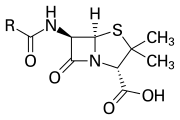
Inelul β-lactamic face parte din structura de bază a mai multor familii de antibiotice , principalele fiind penicilinele , cefalosporinele , carbapenemele și monobactamele , care sunt, prin urmare, numite și antibiotice β-lactamice . Aproape toate aceste antibiotice funcționează prin inhibarea biosintezei peretelui celular bacterian . Acest lucru are un efect letal asupra bacteriilor , deși orice populație de bacterii date va conține de obicei un subgrup care este rezistent la antibiotice β-lactamice. Rezistența bacteriană apare ca urmare a exprimării uneia dintre multele gene pentru producerea de β-lactamaze , o clasă de enzime care deschid inelul β-lactam. Peste 1.800 de enzime β-lactamaze diferite au fost documentate la diferite specii de bacterii. Aceste enzime variază foarte mult în ceea ce privește structura lor chimică și eficiența catalitică. Atunci când populațiile bacteriene au aceste subgrupuri rezistente, tratamentul cu β-lactam poate duce la tulpina rezistentă devenind mai răspândită și, prin urmare, mai virulentă. Antibioticele derivate din β-lactamele pot fi considerate una dintre cele mai importante clase de antibiotice, dar predispuse la rezistență clinică. β-lactamul prezintă proprietățile sale antibiotice prin imitarea substratului natural d-Ala-d-Ala pentru grupul de enzime cunoscut sub numele de proteine de legare a penicilinei (PBP), care au ca funcție de legare încrucișată a părții peptidoglicanului peretelui celular al bacteriile.
Sinteză
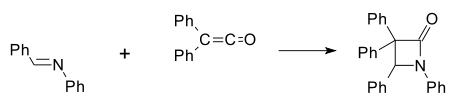
Prima β-lactamă sintetică a fost preparată de Hermann Staudinger în 1907 prin reacția bazei Schiff de anilină și benzaldehidă cu difenilchetină într-o cicloadiție [2 + 2] (Ph indică o grupare funcțională fenil):
Multe metode au fost dezvoltate pentru sinteza β-lactamelor.
Sinteza β-lactam Breckpot produce p-lactame substituite prin ciclizarea beta amino esterilor acizilor prin utilizarea unui reactiv Grignard . Reactivul Mukaiyama este, de asemenea, utilizat în sinteza modificată Breckpot.
Reacții
Datorită tulpinii inelare , β-lactamele sunt mai ușor hidrolizate decât amidele liniare sau lactamele mai mari. Această tulpină este crescută în continuare prin fuziune la un al doilea inel, așa cum se găsește în majoritatea antibioticelor β-lactamice. Această tendință se datorează caracterului amidic al β-lactamei fiind redus de aplanaritatea sistemului. Atomul de azot al unei amide ideală este sp 2 -hybridized datorită rezonanței și sp 2 atomi -hybridized au geometrie legătură plane trigonal . Deoarece o geometrie a legăturii piramidale este forțată asupra atomului de azot de tulpina inelară, rezonanța legăturii amidice este redusă, iar carbonilul devine mai asemănător cetonelor . Premiul Nobel Robert Burns Woodward a descris un parametru h ca o măsură a înălțimii piramidei trigonale definită de azot (ca vârf ) și de cei trei atomi adiacenți ai acestuia. h corespunde puterii legăturii β-lactamice cu un număr mai mic (mai plan; mai mult ca amide ideale) fiind mai puternic și mai puțin reactiv. Monobactamele au valori h între 0,05 și 0,10 angstromi (Å). Cefemele au valori h între 0,20-0,25 Å. Penams au valori cuprinse între 0,40-0,50 Å, în timp ce carbapenemele și clavamele au valori de 0,50-0,60 Å, fiind cele mai reactive dintre β-lactamele spre hidroliză.