Photosystem I - Photosystem I
| Photosystem I | |||||||||
|---|---|---|---|---|---|---|---|---|---|
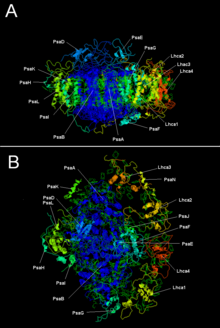 Fotosistemul vegetal I cu LHC I
| |||||||||
| Identificatori | |||||||||
| CE nr. | 1.97.1.12 | ||||||||
| Baze de date | |||||||||
| IntEnz | Vizualizare IntEnz | ||||||||
| BRENDA | Intrare BRENDA | ||||||||
| EXPASy | Vedere NiceZyme | ||||||||
| KEGG | Intrare KEGG | ||||||||
| MetaCyc | cale metabolică | ||||||||
| PRIAM | profil | ||||||||
| Structuri PDB | RCSB PDB PDBe PDBsum | ||||||||
| |||||||||

Fotosistemul I ( PSI , sau plastocianină-feredoxină oxidoreductază ) este unul dintre cele două fotosisteme din reacțiile luminoase fotosintetice ale algelor , plantelor și cianobacteriilor . Fotosistemul I este un complex proteic integral de membrană care folosește energia luminii pentru a cataliza transferul de electroni prin membrana tilacoidă de la plastocianină la feredoxină . În cele din urmă, electronii care sunt transferați de Photosystem I sunt folosiți pentru a produce purtătorul de energie NADPH . Acțiunea combinată a întregului lanț fotosintetic de transport al electronilor produce, de asemenea, o forță proton-motivantă care este utilizată pentru a genera ATP . PSI este compus din mai mult de 110 cofactori , semnificativ mai mult decât Photosystem II .
Istorie
Acest fotosistem este cunoscut sub numele de PSI deoarece a fost descoperit înainte de Photosystem II , deși experimentele viitoare au arătat că Photosystem II este de fapt prima enzimă a lanțului fotosintetic de transport al electronilor. Aspecte ale PSI au fost descoperite în anii 1950, dar semnificațiile acestor descoperiri nu erau încă cunoscute. Louis Duysens a propus pentru prima dată conceptele de Photosystems I și II în 1960 și, în același an, o propunere a lui Fay Bendall și Robert Hill a adunat descoperirile anterioare într-o teorie coezivă a reacțiilor fotosintetice seriale . Ipoteza lui Hill și Bendall a fost ulterior justificată în experimentele efectuate în 1961 de grupurile Duysens și Witt.
Componente și acțiune
Două subunități principale ale PSI, PsaA și PsaB, sunt proteine strâns legate implicate în legarea cofactorilor vitali de transfer de electroni P 700 , Acc, A 0 , A 1 și F x . PsaA și PsaB sunt ambele proteine membranare integrale de 730 până la 750 de aminoacizi care conțin 11 segmente transmembranare . Un grup de fier-sulf [4Fe-4S] numit F x este coordonat de patru cisteine ; două cisteine sunt furnizate fiecare de PsaA și PsaB. Cele două cisteine din fiecare sunt proximale și localizate într-o buclă între segmentele transmembranare nouă și zecea . Un motiv cu fermoar de leucină pare să fie prezent în aval de cisteine și ar putea contribui la dimerizarea PsaA / PsaB. Electronul terminalul acceptori F A și F B , de asemenea , [4Fe-4S] clusterele fier-sulf, sunt situate într - o proteină de 9 kDa numita , care se leagă la PSAC nucleul PsaA / PsaB lângă F X .
| Subunități proteice | Descriere |
|---|---|
| PsaA | Proteine transmembranare mari asociate implicate în legarea P700, A0, A1 și Fx. O parte a familiei de proteine din centrul de reacție fotosintetică . |
| PsaB | |
| PsaC | Centru fier-sulf; apoproteină pentru F a și F b |
| PsaD | Necesar pentru asamblare, ajută la legarea feredoxinei. InterPro : IPR003685 |
| PsaE | InterPro : IPR003375 |
| PsaI | Poate stabiliza PsaL. Stabilizează legarea complexului II de recoltare ușoară . InterPro : IPR001302 |
| PsaJ | InterPro : IPR002615 |
| PsaK | InterPro : IPR035982 |
| PsaL | InterPro : IPR036592 |
| PsaM | InterPro : IPR010010 |
| PsaX | InterPro : IPR012986 |
| complex citocrom b 6 f | Proteine solubile |
| F a | De la PsaC; În lanțul de transport de electroni (ETC) |
| F b | De la PsaC; În ETC |
| F x | De la PsaAB; În ETC |
| Ferredoxină | Purtător de electroni în ETC |
| Plastocianină | Proteine solubile |
| Lipidele | Descriere |
| MGDG II | Monogalactozildiglicerid lipidic |
| PG I | Fosfatidilglicerol fosfolipid |
| PG III | Fosfatidilglicerol fosfolipid |
| PG IV | Fosfatidilglicerol fosfolipid |
| Pigmenți | Descriere |
| Clorofila a | 90 de molecule de pigment în sistemul antenei |
| Clorofila a | 5 molecule de pigment în ETC |
| Clorofila a 0 | Acceptor timpuriu de electroni al clorofilei modificate în ETC |
| Clorofila a ′ | 1 moleculă de pigment în ETC |
| β-caroten | 22 molecule de pigment carotenoid |
| Coenzime și cofactori | Descriere |
| Q K -A | Filochinona de vitamina K 1 acceptatoare timpurie de electroni în ETC |
| Q K -B | Filochinona de vitamina K 1 acceptatoare timpurie de electroni în ETC |
| FNR |
Ferredoxină- NADP+ enzima oxidoreductază |
|
Ca2+ |
Ion calciu |
|
Mg2+ |
Ion magneziu |
Foton
Fotoexcitația moleculelor de pigment din complexul antenei induce transferul de electroni.
Complexul antenei
Complexul antenei este compus din molecule de clorofilă și carotenoide montate pe două proteine. Aceste molecule de pigment transmit energia de rezonanță de la fotoni atunci când devin fotoexcitați. Moleculele antenei pot absorbi toate lungimile de undă ale luminii din spectrul vizibil . Numărul acestor molecule de pigment variază de la organism la organism. De exemplu, cianobacteria Synechococcus elongatus ( Thermosynechococcus elongatus ) are aproximativ 100 de clorofile și 20 de carotenoizi, în timp ce cloroplastele de spanac au în jur de 200 de clorofile și 50 de carotenoizi. Situate în complexul de antene al PSI sunt molecule de clorofilă numite centre de reacție P700 . Energia trecută de moleculele antenei este direcționată către centrul de reacție. Pot exista 120 sau 25 de molecule de clorofilă pe P700.
Centrul de reacție P700
Centrul de reacție P700 este compus din clorofilă modificată care absoarbe cel mai bine lumina la o lungime de undă de 700 nm , cu lungimi de undă mai mari provocând albire. P700 primește energie din moleculele antenei și folosește energia din fiecare foton pentru a ridica un electron la un nivel de energie mai mare. Acești electroni sunt mutați în perechi într-un proces de oxidare / reducere de la P700 la acceptori de electroni. P700 are un potențial electric de aproximativ -1,2 volți . Centrul de reacție este format din două molecule de clorofilă și, prin urmare, este denumit dimer . Se crede că dimerul este compus dintr- o moleculă de clorofilă o și o moleculă de clorofilă a ′ (P700, webber). Cu toate acestea, dacă P700 formează un complex cu alte molecule de antenă, nu mai poate fi un dimer.
Clorofila modificată A 0 și A 1
Cele două molecule de clorofilă modificate sunt acceptori de electroni timpurii în PSI. Sunt prezenți unul pe fiecare parte PsaA / PsaB, formând două ramuri pe care electronii le pot lua pentru a ajunge la F x . A 0 acceptă electroni de la P700, îl trece la A 1 de aceeași parte, care apoi trece electronul la chinonă pe aceeași parte. Specii diferite par să aibă preferințe diferite pentru fiecare ramură A / B.
Filochinona
Filochinonă este următorul acceptorul de electroni devreme în PSI. Filochinona se mai numește uneori vitamina K 1 . Filochinona oxidează A 1 pentru a primi electronul și la rândul său reduce F x pentru a trece electronul la F b și F a . Reducerea lui F x pare a fi etapa de limitare a ratei.
Complex fier-sulf
Trei centre proteice de reacție fier-sulf se găsesc în PSI. Etichetate F x , F a și F b , ele servesc ca relee electronice. F a și F b sunt legate de subunitățile proteice ale complexului PSI și F x este legat de complexul PSI. Diverse experimente au arătat o oarecare diferență între teoriile orientării cofactorului fier-sulf și ordinea de funcționare. Un model este că F x trece un electron la F a , care îl transmite la F b pentru a ajunge la feredoxină.
Ferredoxină
Ferredoxina (Fd) este o proteină solubilă care facilitează reducerea NADP+
către NADPH. Fd se deplasează pentru a transporta un electron fie către un tilacoid singuratic, fie către o enzimă care reduce NADP+
. Membranele tilacoide au un situs de legare pentru fiecare funcție a Fd. Funcția principală a Fd este de a transporta un electron de la complexul fier-sulf la enzima feredoxină - NADP+
reductaza .
Ferredoxină– NADP+
reductază (FNR)
Această enzimă transferă electronul din feredoxina redusă în NADP+
pentru a finaliza reducerea la NADPH. FNR poate accepta, de asemenea, un electron de la NADPH prin legarea acestuia.
Plastocianină
Plastocianina este un purtător de electroni care transferă electronul din citocromul b6f în cofactorul P700 al PSI.
Domeniul proteinei Ycf4
Domeniu de proteine Ycf4 se gaseste pe membrana tilacoidă și este vitală pentru I. fotosistemul Această proteină transmembranară tilacoidă ajută asambla componentele fotosistemul I, fără ea, fotosinteza ar fi ineficientă.
Evoluţie
Datele moleculare arată că PSI a evoluat probabil din fotosistemele bacteriilor cu sulf verde . Fotosistemele bacteriilor cu sulf verde și cele ale cianobacteriilor , algelor și plantelor superioare nu sunt aceleași, totuși există multe funcții analoage și structuri similare. Trei caracteristici principale sunt similare între diferitele fotosisteme. În primul rând, potențialul redox este suficient de negativ pentru a reduce feredoxina. Apoi, centrele de reacție care acceptă electroni includ proteine fier-sulf. În sfârșit, centrele redox în complexele ambelor fotosisteme sunt construite pe un dimer de subunitate proteică. Fotosistemul bacteriilor cu sulf verde conține chiar și aceiași cofactori ai lanțului de transport al electronilor din PSI. Numărul și gradul de asemănări dintre cele două fotosisteme indică cu tărie că PSI este derivat din fotosistemul analog al bacteriilor cu sulf verde.

