Inhibitorul β-lactamazei - β-Lactamase inhibitor
Beta-lactamază sunt o familie de enzime implicate în bacteriene de rezistență la antibiotice beta-lactamice . Aceștia acționează prin ruperea inelului beta-lactamic care permite funcționarea antibioticelor asemănătoare penicilinei . Strategiile pentru combaterea acestei forme de rezistență au inclus dezvoltarea de noi antibiotice beta-lactamice care sunt mai rezistente la scindare și dezvoltarea clasei de inhibitori enzimatici numiți inhibitori beta-lactamazici . Deși inhibitorii β-lactamazei au o activitate antibiotică redusă, aceștia previn degradarea bacteriană a antibioticelor beta-lactamice și astfel extind gama de bacterii împotriva cărora medicamentele sunt eficiente.
Utilizări medicale
Cea mai importantă utilizare a inhibitorilor de beta-lactamază este în tratamentul infecțiilor cunoscute sau considerate a fi cauzate de bacterii gram-negative , deoarece producția de beta-lactamază este un factor important al rezistenței la beta-lactamă la acești agenți patogeni. În schimb, cea mai mare rezistență la beta-lactamă la bacteriile gram-pozitive se datorează variațiilor proteinelor care leagă penicilina care duc la legarea redusă la beta-lactam. Agentul patogen gram-pozitiv Staphylococcus aureus produce beta-lactamaze, dar inhibitorii beta-lactamazelor joacă un rol mai mic în tratamentul acestor infecții deoarece cele mai rezistente tulpini ( Staphylococcus aureus rezistente la meticilină ) folosesc și proteine variante care leagă penicilina.
Mecanism de acțiune
Sistemul de clasificare Ambler grupează enzimele beta-lactamazice cunoscute în patru grupe în funcție de omologia secvenței și de presupuse relații filogenetice. Clasele A, C și D scindează beta-lactamele printr-un mecanism în mai multe etape analog mecanismului serin proteazei . La legare, o grupare serină hidroxil din situsul activ beta-lactamază formează o legătură covalentă tranzitorie la gruparea carbonil a inelului beta-lactamic, scindând inelul beta-lactamic în proces. Într-o a doua etapă, atacul nucleofil al unei molecule de apă scindează legătura covalentă dintre enzimă și gruparea carbonil a beta-lactamului. Acest lucru permite beta-lactamului degradat să se difuzeze și eliberează enzima pentru a procesa molecule suplimentare de beta-lactamă.
Inhibitorii beta-lactamazici disponibili în prezent sunt eficienți împotriva beta-lactamazelor Ambler Clasa A (tazobactam, clavulanat și sulbactam) sau împotriva Ambler Clasa A, C și a unor beta-lactamaze Clasa D (avibactam). La fel ca antibioticele beta-lactamice, acestea sunt procesate de beta-lactamaze pentru a forma un intermediar covalent inițial. Spre deosebire de cazul antibioticelor beta-lactamice, inhibitorii acționează ca substraturi de sinucidere (tazobactam și sulbactam) ceea ce duce în cele din urmă la degradarea beta-lactamazei. Avibactam, pe de altă parte, nu conține un inel beta-lactam (inhibitor non-beta-lactam beta-lactamază) și, în schimb, se leagă reversibil .
Beta-lactamazele Clasa B Ambler scindează beta-lactamele printr-un mecanism similar cu cel al metaloproteazelor . Deoarece nu se formează niciun intermediar covalent, mecanismul de acțiune al inhibitorilor beta-lactamazei comercializați nu se aplică. Astfel, răspândirea tulpinilor bacteriene care exprimă metallo beta-lactamaze, cum ar fi metallo-beta-lactamaza 1 din New Delhi, a generat o îngrijorare considerabilă.
Agenți frecvent utilizați
Inhibitorii β-lactamazei comercializați în prezent nu sunt comercializați ca medicamente individuale. În schimb, acestea sunt co-formulate cu un antibiotic β-lactamic cu un timp de înjumătățire plasmatic similar. Acest lucru se face nu numai pentru confortul dozării, ci și pentru a minimiza dezvoltarea rezistenței care ar putea apărea ca urmare a expunerii variate la unul sau altul medicament. Principalele clase de antibiotice β-lactamice utilizate pentru tratarea infecțiilor bacteriene gram-negative includ (în ordinea aproximativă a rezistenței intrinseci la scindarea de β-lactamaze) peniciline (în special aminopeniciline și ureidopeniciline), cefalosporine de generația a treia și carbapeneme. Variante individuale de β-lactamază pot viza una sau mai multe dintre aceste clase de medicamente și doar un subset va fi inhibat de un anumit inhibitor de β-lactamază. Inhibitorii β-lactamazei extind spectrul util al acestor antibiotice β-lactamice prin inhibarea enzimelor β-lactamazice produse de bacterii pentru a le dezactiva.
- Inhibitori ai β-lactamazei cu nucleul β-lactamului:
- Tebipenem este primul carbapenem care se administrează pe cale orală sub formă de tebipenem-pivoxil. Studiile structurale și cinetice ale tebipenemului sunt disponibile cu M. tuberculosis beta-lactamază (BlaC).
- Acid clavulanic sau clavulanat, de obicei combinat cu amoxicilină ( Augmentin ) sau ticarcilină ( Timentin )
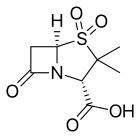
- Sulbactam , de obicei combinat cu ampicilină ( Unasyn ) sau cefoperazonă ( Sulperazon )
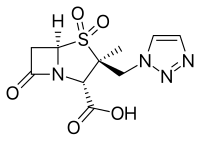
- Tazobactam , de obicei combinat cu piperacilină ( Zosyn și Tazocin )
- Inhibitori ai β-lactamazei cu miez de diazabiciclooctan :
- Avibactam , aprobat în asociere cu ceftazidimă ( Avycaz ), în prezent în curs de studii clinice pentru asociere cu ceftarolină
- Relebactam , utilizat în asociere cu imipenem / cilastatină ( Recarbrio ).
- Inhibitori ai β-lactamazei cu alte tipuri de nuclee non-β-lactamice:
- Vaborbactam , utilizat în combinație cu meropenem ( Vabomere ). Are un miez de acid boronic .
Bacteria care produce beta-lactamază
Bacteriile care pot produce beta-lactamaze includ, dar nu se limitează la:
-
Stafilococ
- MRSA (Staphylococcus aureus rezistent la meticilină)
- Enterobacteriaceae :
- Haemophilus influenzae
- Neisseria gonorrhoeae
- Pseudomonas aeruginosa
- Mycobacterium tuberculosis
Cercetare
Unele bacterii pot produce β-lactamaze cu spectru extins (ESBL), ceea ce face infecția mai dificilă de tratat și conferă rezistență suplimentară penicilinelor , cefalosporinelor și monobactamelor . Derivații acidului boronic se află în prezent în cercetări vaste și extinse ca noi inhibitori ai site-ului activ pentru beta-lactamaze, deoarece conțin un site care imită starea de tranziție prin care trec beta-lactamele atunci când sunt supuse hidrolizei prin beta-lactamaze. S-a constatat că, în general, se încadrează bine în situsul activ al multor beta-lactamaze și au proprietatea convenabilă de a nu putea fi hidrolizați și, prin urmare, devenite inutile. Acesta este un design favorabil al medicamentelor pentru mulți agenți concurenți utilizați clinic, deoarece majoritatea acestora, cum ar fi acidul clavulanic, se hidrolizează și, prin urmare, sunt utile doar pentru o perioadă de timp finită. Acest lucru determină în general necesitatea unei concentrații mai mari de inhibitor competitiv decât ar fi necesar într-un inhibitor nehidrolizabil. Diferenți derivați ai acidului boronic au potențialul de a fi adaptați la numeroasele izoforme diferite de beta-lactamaze și, prin urmare, au potențialul de a restabili puterea antibioticelor beta-lactamice.
Referințe
linkuri externe
- Xu H, Hazra S, Blanchard JS (iunie 2012). „NXL104 inhibă ireversibil β-lactamaza din Mycobacterium tuberculosis” . Biochimie . 51 (22): 4551-7. doi : 10.1021 / bi300508r . PMC 3448018 . PMID 22587688 .
- Kurz SG, Wolff KA, Hazra S, Bethel CR, Hujer AM, Smith KM, Xu Y, Tremblay LW, Blanchard JS, Nguyen L, Bonomo RA (decembrie 2013). „Poate substituțiile rezistente la inhibitori în Mycobacterium tuberculosis β-Lactamase BlaC să conducă la rezistență la clavulanat ?: o rațiune biochimică pentru utilizarea combinațiilor de inhibitori de β-lactam-β-lactamază” . Agenți antimicrobieni și chimioterapie . 57 (12): 6085-96. doi : 10.1128 / AAC.01253-13 . PMC 3837893 . PMID 24060876 .