4,7-diclorochinolină - 4,7-Dichloroquinoline

|
|
| Numele | |
|---|---|
|
Numele IUPAC preferat
4,7-diclorochinolină |
|
| Identificatori | |
|
Model 3D ( JSmol )
|
|
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard |
100,001,559 |
| Numărul CE | |
|
PubChem CID
|
|
| UNII | |
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Proprietăți | |
| C 9 H 5 Cl 2 N | |
| Masă molară | 198,05 g · mol −1 |
| Aspect | pudră albă |
| Punct de topire | 87 ° C (189 ° F; 360 K) |
| Punct de fierbere | 317 ° C (603 ° F; 590 K) |
| Pericole | |
| Pictograme GHS |
 
|
| GHS Cuvânt de avertizare | Avertizare |
| H315 , H317 , H319 , H335 , H411 | |
| P261 , P264 , P271 , P272 , P273 , P280 , P302 + 352 , P304 + 340 , P305 + 351 + 338 , P312 , P321 , P332 + 313 , P333 + 313 , P337 + 313 , P362 , P363 , P391 , P403 + 233 , P405 , P501 | |
| Punct de aprindere | 164 ° C (327 ° F; 437 K) |
| Referințe infobox | |
4,7-Diclorochinolina este un compus heterociclic cu două inele utilizat ca intermediar chimic pentru medicamentele antimalarice ale aminochinolinei , inclusiv amodiaquina , clorochina și hidroxiclorochina .
Sinteză
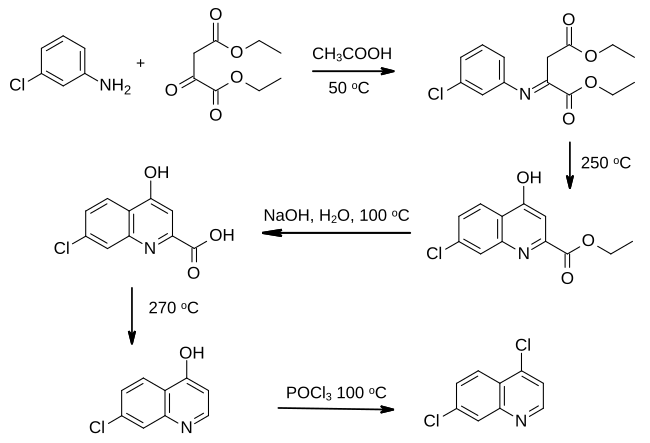
4,7-diclorochinolina a fost raportată pentru prima dată într-un brevet depus de IG Farben în 1937. Cu toate acestea, sinteza sa nu a fost investigată în detaliu până când cloroquina nu a fost dezvoltată ca medicament antimalaric. O cale de pornirea intermediar din 3-cloranilina a fost dezvoltat de chimisti de la Winthrop Chemical Co .
Anilină substituită este condensat cu dietil esterul al acidului oxaloacetică în condiții acide blânde, formând o imină , care este ciclizată pentru a forma inelul piridinic prin încălzirea în ulei mineral. Urmează hidroliza și decarboxilarea , înainte ca gruparea hidroxi din poziția 4 să fie transformată în a doua grupare clor folosind clorură de fosforil .
Disponibilitatea 4,7-diclorochinolinei a permis investigarea analogilor structurali alternativi de tipul 4-aminoquinolinei , ceea ce a condus la descoperirea hidroxiclorochinei în 1949. Până la acel moment, procesele de fabricație a clorochinei au fost stabilite pentru a permite utilizarea sa pe scară largă. 4,7-Diclorochinolina a fost, de asemenea, preparată prin reacția Gould – Jacobs utilizând o metodă alternativă de construire a inelului piridinic din 3-cloroanilină.
Reacții
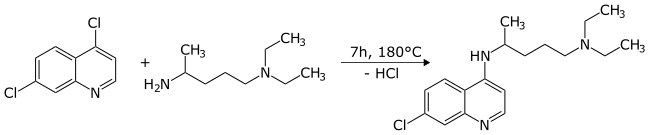
Atomul de clor din poziția 4 din inelul piridinic este mult mai reactiv în reacțiile de substituție nucleofilă aromatică decât clorul din inelul benzenic . Ca urmare, poate fi înlocuit selectiv pentru a forma derivate în acea poziție. O reacție tipică cu o amină primară specifică dă clorochină cu randament ridicat:
Utilizări
În afară de utilizarea sa în fabricarea antimalaricelor deja descrise, 4,7-diclorochinolina are un interes continuu ca intermediar pentru noii candidați la medicamente.
Referințe
Lecturi suplimentare
- Slater, Leo (9 ianuarie 2009). Război și boli: cercetări biomedicale asupra malariei în secolul al XX-lea . ISBN 9780813546469.