Hemodializa - Hemodialysis
| Hemodializa | |
|---|---|
 Aparat de hemodializă
| |
| Alte nume | Dializă la rinichi |
| Specialitate | nefrologie |
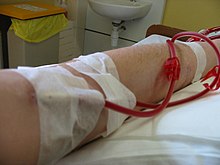
Hemodializa , de asemenea hemodializa ortografiată sau pur și simplu dializa , este un proces de purificare a sângelui unei persoane ai cărei rinichi nu funcționează normal. Acest tip de dializă realizează îndepărtarea extracorporală a deșeurilor cum ar fi creatinina și ureea și apa liberă din sânge atunci când rinichii se află într-o stare de insuficiență renală . Hemodializa este una dintre cele trei terapii de substituție renală (celelalte două fiind transplantul de rinichi și dializa peritoneală ). O metodă alternativă pentru separarea extracorporală a componentelor sanguine, cum ar fi plasma sau celulele, este afereza .
Hemodializa poate fi o terapie ambulatorie sau internată . Hemodializa de rutină se desfășoară într-un ambulatoriu pentru dializă, fie într-o cameră special construită într-un spital , fie într-o clinică dedicată, independentă. Mai rar hemodializa se face acasă . Tratamentele de dializă într-o clinică sunt inițiate și gestionate de personal specializat format din asistenți medicali și tehnicieni; tratamentele de dializă la domiciliu pot fi auto-inițiate și gestionate sau realizate împreună cu asistența unui ajutor instruit, care este de obicei un membru al familiei.
Utilizări medicale
Hemodializa este alegerea terapiei de substituție renală pentru pacienții care au nevoie de dializă acută și pentru mulți pacienți ca terapie de întreținere. Oferă o eliminare rapidă excelentă a substanțelor dizolvate.
Un nefrolog (specialist în rinichi medical) decide când este necesară hemodializa și diferiții parametri pentru un tratament de dializă. Acestea includ frecvența (câte tratamente pe săptămână), durata fiecărui tratament și debitele de sânge și soluție de dializă, precum și dimensiunea dializatorului. Compoziția soluției de dializă este, de asemenea, ajustată uneori în funcție de nivelurile sale de sodiu, potasiu și bicarbonat. În general, cu cât este mai mare dimensiunea corpului unei persoane, cu atât mai multă dializă va avea nevoie. În America de Nord și Marea Britanie , tratamentele de 3-4 ore (uneori până la 5 ore pentru pacienții mai mari) administrate de 3 ori pe săptămână sunt tipice. Ședințele de două ori pe săptămână sunt limitate la pacienții care au o funcție renală substanțială reziduală. Patru ședințe pe săptămână sunt deseori prescrise pacienților mai mari, precum și pacienților care au probleme cu supraîncărcarea lichidelor . În cele din urmă, există un interes tot mai mare pentru hemodializa zilnică scurtă , care este de 1,5 - 4 ore sesiuni date de 5-7 ori pe săptămână, de obicei acasă. Există, de asemenea, interes pentru dializa nocturnă , care implică dializarea unui pacient, de obicei acasă, timp de 8-10 ore pe noapte, 3-6 nopți pe săptămână. Dializa nocturnă în centru, de 3-4 ori pe săptămână, este oferită și la o mână de unități de dializă din Statele Unite .
Efecte adverse
Dezavantaje
- Restricționează independența, deoarece persoanele care urmează această procedură nu pot călători din cauza disponibilității aprovizionării
- Necesită mai multe surse precum calitatea ridicată a apei și electricitate
- Necesită o tehnologie fiabilă, cum ar fi aparatele de dializă
- Procedura este complicată și necesită ca îngrijitorii să aibă mai multe cunoștințe
- Necesită timp pentru instalarea și curățarea mașinilor de dializă și cheltuieli cu mașinile și personalul asociat
Complicații
Schimbări de lichid
Hemodializa implică adesea îndepărtarea lichidelor (prin ultrafiltrare ), deoarece majoritatea pacienților cu insuficiență renală trec urină mică sau deloc. Efectele secundare cauzate de îndepărtarea prea multor lichide și / sau îndepărtarea lichidului prea rapid includ tensiune arterială scăzută , oboseală , dureri în piept, crampe la picioare, greață și dureri de cap . Aceste simptome pot apărea în timpul tratamentului și pot persista după tratament; uneori sunt denumiți în mod colectiv mahmureală de dializă sau spălare de dializă. Severitatea acestor simptome este de obicei proporțională cu cantitatea și viteza de eliminare a lichidului. Cu toate acestea, impactul unei cantități date sau a unei rate de eliminare a lichidului poate varia foarte mult de la o persoană la alta și de la o zi la alta. Aceste reacții adverse pot fi evitate și / sau severitatea lor poate fi redusă prin limitarea aportului de lichide între tratamente sau creșterea dozei de dializă, de exemplu dializarea mai des sau mai mult pe tratament decât standardul de trei ori pe săptămână, 3-4 ore pe program de tratament.
Deoarece hemodializa necesită acces la sistemul circulator, pacienții care fac hemodializă își pot expune sistemul circulator la microbi , ceea ce poate duce la bacteremie , la o infecție care afectează valvele cardiace ( endocardită ) sau la o infecție care afectează oasele ( osteomielită ). Riscul de infecție variază în funcție de tipul de acces utilizat (vezi mai jos). De asemenea, poate apărea sângerare, iar riscul variază în funcție de tipul de acces utilizat. Infecțiile pot fi reduse la minimum prin respectarea strictă a celor mai bune practici de combatere a infecțiilor .
Dislocarea acului venos
Dislocarea venoasă a acului (VND) este o complicație fatală a hemodializei în care pacientul suferă pierderi rapide de sânge din cauza unei atașări șovăitoare a acului la punctul de acces venos.
Heparina nefracționată (UHF) este cel mai frecvent utilizat anticoagulant în hemodializă, deoarece este în general bine tolerat și poate fi inversat rapid cu sulfat de protamină . Cu toate acestea, heparina cu greutate moleculară mică (LMWH) devine din ce în ce mai populară și este acum norma în vestul Europei. În comparație cu UHF, LMWH are avantajul unui mod de administrare mai ușor și a sângerării reduse, dar efectul nu poate fi inversat cu ușurință. Heparina poate provoca rareori un număr scăzut de trombocite datorită unei reacții numite trombocitopenie indusă de heparină (HIT) . La astfel de pacienți, pot fi utilizate anticoagulante alternative. Riscul de HIT este mai mic cu LMWH comparativ cu UHF. Chiar dacă HIT determină un număr scăzut de trombocite, poate predispune paradoxal tromboza. La pacienții cu risc crescut de sângerare, dializa se poate face fără anticoagulare.
Sindromul de primă utilizare
Sindromul de primă utilizare este o reacție anafilactică rară, dar severă la rinichiul artificial . Simptomele sale includ strănut, respirație șuierătoare, dificultăți de respirație, dureri de spate, dureri în piept sau moarte subită. Poate fi cauzat de sterilizant rezidual în rinichiul artificial sau materialul membranei în sine. În ultimii ani, incidența sindromului de primă utilizare a scăzut, datorită utilizării crescute a iradierii gamma , a sterilizării cu abur sau a radiației cu fascicul de electroni în locul sterilizantelor chimice și a dezvoltării de noi membrane semipermeabile cu o biocompatibilitate mai mare . Trebuie luate întotdeauna în considerare noile metode de prelucrare a componentelor dializei acceptate anterior. De exemplu, în 2008, o serie de reacții de primă utilizare, inclusiv decese, au apărut din cauza heparinei contaminate în timpul procesului de fabricație cu sulfat de condroitină suprasulfatat .
Cardiovascular
Complicațiile pe termen lung ale hemodializei includ amiloidoză asociată hemodializei , neuropatie și diferite forme de boli de inimă . Creșterea frecvenței și a duratei tratamentelor sa dovedit a îmbunătăți supraîncărcarea de lichide și mărirea inimii, care este frecvent observată la acești pacienți. Datorită acestor complicații, prevalența utilizării medicamentelor complementare și alternative este ridicată în rândul pacienților supuși hemodializei.
Deficitul de vitamine
Deficitul de folat poate apărea la unii pacienți cu hemodializă.
Dezechilibre electrolitice
Deși un fluid dializat, care este o soluție care conține electroliți diluați, este utilizat pentru filtrarea sângelui, hemodializa poate provoca un dezechilibru electrolitic. Aceste dezechilibre pot proveni din concentrații anormale de potasiu ( hipokaliemie , hiperkaliemie ) și sodiu ( hiponatremie , hipernatremie ). Aceste dezechilibre electrolitice sunt asociate cu creșterea mortalității cardiovasculare.
Mecanism și tehnică
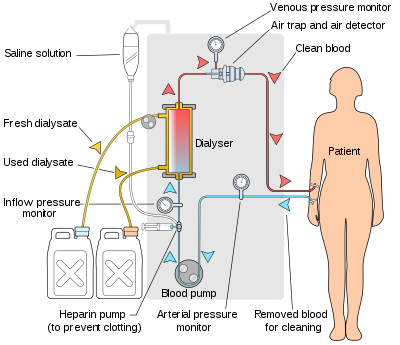
Principiul hemodializei este același cu celelalte metode de dializă ; implică difuzia de substanțe dizolvate pe o membrană semipermeabilă. Hemodializa utilizează fluxul de contracurent , în care dializatul curge în direcția opusă fluxului de sânge din circuitul extracorporeal . Fluxul contracurent menține gradientul de concentrație la nivelul membranei la maximum și crește eficiența dializei.
Îndepărtarea lichidului ( ultrafiltrare ) se realizează prin modificarea presiunii hidrostatice a compartimentului dializat, determinând deplasarea apei libere și a unor substanțe dizolvate dizolvate de-a lungul membranei de-a lungul unui gradient de presiune creat.
Soluția de dializă utilizată poate fi o soluție sterilizată de ioni minerali și se numește dializat. Ureea și alte produse reziduale, inclusiv potasiu și fosfat, se difuzează în soluția de dializă. Cu toate acestea, concentrațiile de sodiu și clorură sunt similare cu cele ale plasmei normale pentru a preveni pierderea. Bicarbonatul de sodiu este adăugat într-o concentrație mai mare decât plasma pentru a corecta aciditatea sângelui. O cantitate mică de glucoză este, de asemenea, frecvent utilizată. Concentrația de electroliți din dializat este ajustată în funcție de starea pacientului înainte de dializă. Dacă la dializat se adaugă o concentrație ridicată de sodiu, pacientul poate deveni sete și ajunge să acumuleze lichide corporale, ceea ce poate duce la leziuni cardiace. Dimpotrivă, concentrațiile scăzute de sodiu în soluția de dializat au fost asociate cu o tensiune arterială scăzută și creșterea în greutate intradialytic, care sunt markeri ai rezultatelor îmbunătățite. Cu toate acestea, beneficiile utilizării unei concentrații scăzute de sodiu nu au fost încă demonstrate, deoarece acești pacienți pot suferi și crampe, hipotensiune intradialytică și sodiu scăzut în ser, care sunt simptome asociate cu un risc ridicat de mortalitate.
Rețineți că acesta este un proces diferit de tehnica conexă de hemofiltrare .
Acces
Trei metode primare sunt utilizate pentru a avea acces la sânge pentru hemodializă: un cateter intravenos, o fistulă arteriovenoasă (AV) și o grefă sintetică. Tipul de acces este influențat de factori precum evoluția așteptată a insuficienței renale a pacientului și starea vasculaturii acestuia. Pacienții pot avea proceduri multiple de acces, de obicei, deoarece o fistulă AV sau o grefă se maturizează și un cateter este încă utilizat. Amplasarea unui cateter se face de obicei sub sedare ușoară, în timp ce fistulele și grefele necesită o operație.
Tipuri
Există trei tipuri de hemodializă: hemodializa convențională, hemodializa zilnică și hemodializa nocturnă. Mai jos este o adaptare și un rezumat dintr-o broșură a Spitalului Ottawa.
Hemodializa convențională
Hemodializa convențională se face de obicei de trei ori pe săptămână, timp de aproximativ trei până la patru ore pentru fiecare tratament (Uneori cinci ore pentru pacienții mai mari), timp în care sângele pacientului este extras printr-un tub cu o rată de 200-400 ml / min. Tubul este conectat la un ac de calibru 15, 16 sau 17 introdus în fistula sau grefa de dializă sau conectat la un orificiu al cateterului de dializă . Sângele este apoi pompat prin dializator și apoi sângele procesat este pompat înapoi în fluxul sanguin al pacientului printr-un alt tub (conectat la un al doilea ac sau orificiu). În timpul procedurii, tensiunea arterială a pacientului este atent monitorizată și, dacă aceasta scade, sau pacientul prezintă orice alte semne de volum scăzut de sânge, cum ar fi greață, asistentul de dializă poate administra lichid suplimentar prin aparat. În timpul tratamentului, întregul volum de sânge al pacientului (aproximativ 5000 cc) circulă prin aparat la fiecare 15 minute. În timpul acestui proces, pacientul cu dializă este expus la o săptămână de apă pentru o persoană obișnuită.
Hemodializa zilnică
Hemodializa zilnică este de obicei utilizată de acei pacienți care își fac propria dializă acasă. Este mai puțin stresant (mai blând), dar necesită un acces mai frecvent. Acest lucru este simplu cu catetere, dar mai problematic cu fistulele sau grefele. „Tehnica butonierei” poate fi utilizată pentru fistule care necesită acces frecvent. Hemodializa zilnică se face de obicei timp de 2 ore șase zile pe săptămână.
Hemodializa nocturnă
Procedura hemodializei nocturne este similară cu hemodializa convențională, cu excepția cazului în care se efectuează trei până la șase nopți pe săptămână și între șase și zece ore pe ședință în timp ce pacientul doarme.
Echipament
Aparatul de hemodializă pompează sângele pacientului și dializatul prin dializator. Cele mai noi aparate de dializă de pe piață sunt extrem de computerizate și monitorizează continuu o serie de parametri critici pentru siguranță, inclusiv debitul de sânge și dializat; conductivitatea, temperatura și pH-ul soluției de dializă; și analiza dializatului pentru evidența scurgerilor de sânge sau a prezenței aerului. Orice citire care se află în afara intervalului normal declanșează o alarmă sonoră pentru a alerta tehnicianul de îngrijire a pacientului care monitorizează pacientul. Producătorii de aparate de dializă includ companii precum Nipro , Fresenius , Gambro , Baxter, B. Braun , NxStage și Bellco.
Sistem de apa
Un sistem extins de purificare a apei este absolut critic pentru hemodializă. Deoarece pacienții cu dializă sunt expuși la cantități mari de apă, care este amestecată cu concentrat de dializat pentru a forma dializatul, chiar și urme de contaminanți minerali sau endotoxine bacteriene se pot filtra în sângele pacientului. Deoarece rinichii deteriorați nu își pot îndeplini funcția prevăzută de îndepărtare a impurităților, ionii introduși în sânge prin apă se pot acumula până la niveluri periculoase, provocând numeroase simptome sau moarte . Aluminiu, cloramină , fluor, cupru și zinc, precum și fragmente bacteriene și endotoxine, toate au cauzat probleme în acest sens.
Din acest motiv, apa utilizată în hemodializă este purificată cu atenție înainte de utilizare. Inițial, este filtrat și ajustat la temperatură și pH-ul său este corectat prin adăugarea unui acid sau a unei baze. Se pot adăuga tampoane chimice, cum ar fi bicarbonatul și lactatul, pentru a regla pH-ul dializatului. Ambele tampoane pot stabiliza pH-ul soluției la un nivel fiziologic fără efecte negative asupra pacientului. Există unele dovezi ale unei reduceri a incidenței problemelor cardiace și sanguine și a evenimentelor de tensiune arterială crescută atunci când se utilizează bicarbonat ca tampon de pH comparativ cu lactatul. Cu toate acestea, ratele mortalității după utilizarea ambelor tampoane nu prezintă o diferență semnificativă.
Soluția de dializat este apoi înmuiată. Apoi, apa se trece printr-un rezervor care conține cărbune activ pentru a absorbi contaminanții organici. Purificarea primară se face apoi prin forțarea apei printr-o membrană cu pori foarte mici, așa-numita membrană cu osmoză inversă . Acest lucru lasă apa să treacă, dar reține chiar și solutii foarte mici, cum ar fi electroliții. Îndepărtarea finală a restului de electroliți se face prin trecerea apei printr-un rezervor cu rășini schimbătoare de ioni, care elimină anionii sau cationii rămași și îi înlocuiesc cu ioni hidroxil și respectiv hidrogen, lăsând apă ultrapură.
Chiar și acest grad de purificare a apei poate fi insuficient. Tendința în ultima vreme este de a trece această apă finală purificată (după amestecarea cu concentrat de dializat) printr-o membrană dializator. Aceasta oferă un alt strat de protecție prin îndepărtarea impurităților, în special a celor de origine bacteriană, care s-ar fi putut acumula în apă după trecerea acesteia prin sistemul original de purificare a apei.
Odată ce apa purificată este amestecată cu concentrat de dializat, conductivitatea acesteia crește, deoarece apa care conține ioni încărcați conduce electricitatea. În timpul dializei, conductivitatea soluției de dializă este monitorizată continuu pentru a se asigura că apa și concentratul de dializat sunt amestecate în proporțiile corespunzătoare. Atât soluția de dializă excesiv concentrată, cât și soluția diluată excesiv pot provoca probleme clinice severe.
Dializator
Dializatorul este piesa de echipament care filtrează de fapt sângele. Aproape toate dializatoarele utilizate astăzi sunt din varietatea de fibre goale. Un pachet cilindric de fibre goale, ai cărui pereți sunt compuși din membrană semipermeabilă, este ancorat la fiecare capăt în compusul de ghiveci (un fel de lipici). Acest ansamblu este apoi pus într-o carcasă cilindrică din plastic transparent cu patru deschideri. O deschidere sau orificiu de sânge la fiecare capăt al cilindrului comunică cu fiecare capăt al mănunchiului de fibre goale. Aceasta formează „compartimentul de sânge” al dializatorului. Alte două orificii sunt tăiate în lateralul cilindrului. Acestea comunică cu spațiul din jurul fibrelor goale, „compartimentul dializat”. Sângele este pompat prin orificiile de sânge prin acest pachet de tuburi foarte subțiri asemănătoare capilarelor , iar dializatul este pompat prin spațiul care înconjoară fibrele. Gradienții de presiune sunt aplicați atunci când este necesar pentru a muta fluidul din sânge în compartimentul dializat.
Membrană și flux
Membranele dializatorului vin cu diferite dimensiuni ale porilor. Cei cu dimensiuni mai mici ale porilor sunt numiți „cu flux scăzut”, iar cei cu dimensiuni mai mari ai porilor sunt numiți „cu flux mare”. Unele molecule mai mari, cum ar fi beta-2-microglobulina, nu sunt deloc îndepărtate cu dializatoare cu flux redus; în ultimul timp, tendința a fost de a utiliza dializatoare cu flux ridicat. Cu toate acestea, astfel de dializatoare necesită aparate de dializă mai noi și o soluție de dializă de înaltă calitate pentru a controla în mod corespunzător rata de îndepărtare a lichidului și pentru a preveni refluxul impurităților soluției de dializă în pacient prin membrană.
Membranele dializatorului erau fabricate în principal din celuloză (derivată din bumbac). Suprafața acestor membrane nu era foarte biocompatibilă, deoarece grupările hidroxil expuse ar activa complementul din sângele care trece prin membrană. Prin urmare, membrana celulozică de bază, „nesubstituită” a fost modificată. O schimbare a fost acoperirea acestor grupări hidroxil cu grupări acetat (acetat de celuloză); un altul a fost amestecarea unor compuși care ar inhiba activarea complementului la suprafața membranei (celuloză modificată). Membranele originale de „celuloză nesubstituită” nu mai sunt utilizate pe scară largă, în timp ce acetat de celuloză și dializatoare de celuloză modificate sunt încă utilizate. Membranele celulozice pot fi realizate fie în configurație cu flux scăzut, fie cu flux ridicat, în funcție de mărimea porilor lor.
Un alt grup de membrane este realizat din materiale sintetice, folosind polimeri precum poliariletersulfona , poliamida , polivinilpirolidona , policarbonatul și poliacrilonitrilul . Aceste membrane sintetice activează complementul într-un grad mai mic decât membranele de celuloză nesubstituite. Cu toate acestea, acestea sunt, în general, mai hidrofobe, ceea ce duce la o adsorbție crescută a proteinelor la suprafața membranei, ceea ce la rândul său poate duce la activarea sistemului complementar. Membranele sintetice pot fi realizate fie în configurație cu flux scăzut, fie cu flux ridicat, dar majoritatea sunt cu flux ridicat.
Nanotehnologia este utilizată în unele dintre cele mai recente membrane cu flux ridicat pentru a crea o dimensiune uniformă a porilor. Scopul membranelor cu flux ridicat este de a trece molecule relativ mari, cum ar fi beta-2-microglobulină (MW 11.600 daltoni), dar nu de a trece albumina (MW ~ 66.400 daltoni). Fiecare membrană are pori într-o gamă de dimensiuni. Pe măsură ce mărimea porilor crește, unii dializatori cu flux ridicat încep să lase albumina să treacă din sânge în dializat. Acest lucru este considerat a fi nedorit, deși o școală de gândire susține că îndepărtarea unei anumite albumine poate fi benefică în ceea ce privește eliminarea toxinelor uremice legate de proteine.
Fluxul și rezultatul membranei
Dacă utilizarea unui dializator cu flux ridicat îmbunătățește rezultatele pacienților este oarecum controversat, dar mai multe studii importante au sugerat că are beneficii clinice. Studiul HEMO finanțat de NIH a comparat supraviețuirea și spitalizările la pacienții randomizați la dializă cu membrane cu flux scăzut sau cu flux ridicat. Deși rezultatul primar (mortalitatea pentru toate cauzele) nu a atins semnificația statistică în grupul randomizat pentru a utiliza membrane cu flux ridicat, mai multe rezultate secundare au fost mai bune în grupul cu flux ridicat. O analiză recentă Cochrane a concluzionat că beneficiul alegerii membranei asupra rezultatelor nu a fost încă demonstrat. Un studiu randomizat colaborativ din Europa, studiul MPO (Membrane Permeabilities Outcomes), care compară mortalitatea la pacienții care tocmai au început dializa folosind fie membranele cu flux ridicat, fie cele cu flux scăzut, a găsit o tendință nesemnificativă de supraviețuire îmbunătățită la cei care utilizează membrane cu flux ridicat și un beneficiu de supraviețuire la pacienții cu niveluri mai scăzute de albumină serică sau la diabetici.
Flux de membrană și amiloidoză beta-2-microglobulină
Membranele de dializă cu flux ridicat și / sau hemodiafiltrarea on-line intermitentă (IHDF) pot fi, de asemenea, benefice în reducerea complicațiilor acumulării de beta-2-microglobulină. Deoarece beta-2-microglobulina este o moleculă mare, cu o greutate moleculară de aproximativ 11.600 daltoni, nu trece deloc prin membranele de dializă cu flux scăzut. Beta-2-M este îndepărtat cu dializă cu flux ridicat, dar este îndepărtat și mai eficient cu IHDF. După câțiva ani (de obicei cel puțin 5-7), pacienții care fac hemodializă încep să dezvolte complicații din acumularea de beta-2-M, inclusiv sindromul tunelului carpian, chisturile osoase și depunerile acestui amiloid în articulații și alte țesuturi. Amiloidoza beta-2-M poate provoca complicații foarte grave, inclusiv spondiloartropatia , și este adesea asociată cu probleme ale articulațiilor umărului. Studiile observaționale din Europa și Japonia au sugerat că utilizarea membranelor cu flux ridicat în modul de dializă, sau IHDF, reduce complicațiile beta-2-M în comparație cu dializa regulată folosind o membrană cu flux scăzut.
Dimensiunea și eficiența dializatorului
Dializatoarele vin în multe dimensiuni diferite. Un dializator mai mare cu o suprafață mai mare a membranei (A) va elimina, de obicei, mai multe substanțe dizolvate decât un dializator mai mic, în special la debitul sanguin ridicat. Acest lucru depinde și de coeficientul de permeabilitate a membranei K 0 pentru solutul în cauză. Deci, eficiența dializatorului este de obicei exprimată ca K 0 A - produsul coeficientului și zonei de permeabilitate. Majoritatea dializatoarelor au suprafețe de membrană de 0,8 până la 2,2 metri pătrați și valori de K 0 A variind de la aproximativ 500 la 1500 mL / min. K 0 A , exprimat în ml / min, poate fi considerat drept clearance-ul maxim al unui dializator la debituri foarte mari de sânge și dializat.
Reutilizarea dializatoarelor
Dializorul poate fi fie aruncat după fiecare tratament, fie reutilizat. Reutilizarea necesită o procedură extinsă de dezinfecție la nivel înalt. Dializatoarele refolosite nu sunt împărțite între pacienți. A existat o controversă inițială cu privire la faptul dacă refolosirea dializatoarelor a agravat rezultatele pacienților. Consensul de astăzi este că reutilizarea dializatoarelor, dacă se face cu atenție și corect, produce rezultate similare cu utilizarea unică a dializatoarelor.
Dialyzer Reuse este o practică existentă de la inventarea produsului. Această practică include curățarea unui dializator folosit pentru a fi reutilizat de mai multe ori pentru același pacient. Clinicile de dializă reutilizează dializatoarele pentru a deveni mai economice și pentru a reduce costurile ridicate ale dializei cu o singură utilizare, care poate fi extrem de costisitoare și risipitoare. Dializatoarele de unică folosință sunt inițiate o singură dată și apoi aruncate afară, creând o cantitate mare de deșeuri biologice, fără milă de reducerea costurilor. Dacă se face corect, refolosirea dializatorului poate fi foarte sigură pentru pacienții cu dializă.
Există două moduri de reutilizare a dializatoarelor, manuală și automată. Reutilizarea manuală implică curățarea manuală a unui dializator. Dializatorul este semi-demontat, apoi spălat în mod repetat înainte de a fi clătit cu apă. Se păstrează apoi cu un dezinfectant lichid (PAA) timp de peste 18 ore până la următoarea utilizare. Deși multe clinici din afara SUA folosesc această metodă, unele clinici trec la un proces mai automat / raționalizat pe măsură ce practica de dializă avansează. Cea mai nouă metodă de reutilizare automată este realizată prin intermediul unui dispozitiv medical care a început la începutul anilor 1980. Aceste dispozitive sunt benefice clinicilor de dializă care practică refolosirea - în special pentru entitățile clinice mari de dializă - deoarece permit mai multe cicluri de spate în spate pe zi. Dializatorul este mai întâi curățat în prealabil de către un tehnician, apoi curățat automat de mașină printr-un proces de cicluri de etape până când este în cele din urmă umplut cu dezinfectant lichid pentru depozitare. Deși refolosirea automată este mai eficientă decât refolosirea manuală, tehnologia mai nouă a stârnit și mai multe progrese în procesul de reutilizare. Când este reutilizat de peste 15 ori cu metodologia actuală, dializatorul poate pierde B2m, clearance-ul moleculei medii și integritatea structurii porilor de fibre, ceea ce are potențialul de a reduce eficacitatea sesiunii de dializă a pacientului. În prezent, începând cu 2010, o tehnologie mai nouă și mai avansată de reprocesare a dovedit capacitatea de a elimina complet procesul de pre-curățare manuală și a dovedit, de asemenea, potențialul de a regenera (restabili complet) toate funcțiile unui dializator la niveluri care sunt aproximativ echivalente cu de unică folosință pentru mai mult de 40 de cicluri. Pe măsură ce ratele de rambursare medicală încep să scadă și mai mult, multe clinici de dializă continuă să funcționeze eficient cu programe de reutilizare, mai ales că procesul este mai ușor și mai raționalizat decât înainte.
Epidemiologie
Hemodializa a fost una dintre cele mai frecvente proceduri efectuate în spitalele din SUA în 2011, care a avut loc în 909.000 de sejururi (o rată de 29 de sejururi la 10.000 de locuitori). Aceasta a reprezentat o creștere de 68% față de 1997, când au existat 473.000 de sejururi. A fost a cincea cea mai frecventă procedură la pacienții cu vârsta cuprinsă între 45 și 64 de ani.
Istorie
Mulți au jucat un rol în dezvoltarea dializei ca tratament practic pentru insuficiența renală, începând cu Thomas Graham din Glasgow , care a prezentat pentru prima dată principiile transportului solutului pe o membrană semipermeabilă în 1854. Rinichiul artificial a fost dezvoltat pentru prima dată de Abel , Rountree și Turner în 1913, prima hemodializă la o ființă umană a fost de Haas (28 februarie 1924), iar rinichiul artificial a fost transformat într-un aparat util clinic de Kolff în 1943 - 1945. Această cercetare a arătat că viața ar putea fi prelungită la pacienții care mor de insuficiență renală .
Willem Kolff a fost primul care a construit un dializator funcțional în 1943. Primul pacient tratat cu succes a fost o femeie în vârstă de 67 de ani în comă uremică care și-a recăpătat cunoștința după 11 ore de hemodializă cu dializatorul lui Kolff în 1945. La momentul creării sale, Scopul lui Kolff a fost de a oferi sprijin de viață în timpul recuperării după insuficiență renală acută. După încheierea celui de-al doilea război mondial , Kolff a donat cele cinci dializatoare pe care le făcuse spitalelor din întreaga lume, inclusiv Spitalul Mount Sinai, New York . Kolff ia dat un set de planuri pentru aparatul său de hemodializă lui George Thorn la Spitalul Peter Bent Brigham din Boston . Acest lucru a dus la fabricarea următoarei generații de dializator Kolff, un aparat de dializă Kolff-Brigham din oțel inoxidabil .
Potrivit lui McKellar (1999), o contribuție semnificativă la terapiile renale a fost adusă de chirurgul canadian Gordon Murray cu asistența a doi medici, un student la chimie și un personal de cercetare. Lucrarea lui Murray a fost condusă simultan și independent de cea a lui Kolff. Lucrarea lui Murray a condus la primul rinichi artificial de succes construit în America de Nord în 1945–46, care a fost folosit cu succes pentru a trata o femeie de 26 de ani dintr-o comă uremică din Toronto. Dializatorul „Murray-Roschlau” de generația a doua mai puțin brut, mai compact, a fost inventat în 1952–53, ale cărui modele au fost furate de imigrantul german Erwin Halstrup și au trecut ca ale sale („rinichiul artificial Halstrup – Baumann”) .
În anii 1950, invenția dializatorului de către Willem Kolff a fost utilizată pentru insuficiența renală acută, dar nu a fost văzută ca un tratament viabil pentru pacienții cu boală renală cronică în stadiul 5 (ERC). La acea vreme, medicii credeau că este imposibil ca pacienții să facă dializă pe termen nelimitat din două motive. În primul rând, au crezut că niciun dispozitiv creat de om nu poate înlocui funcția rinichilor pe termen lung. În plus, un pacient supus dializei a suferit venele și arterele deteriorate, astfel încât, după mai multe tratamente, a devenit dificil să găsească un vas pentru a accesa sângele pacientului.
Rinichiul original Kolff nu a fost foarte util din punct de vedere clinic, deoarece nu a permis eliminarea excesului de lichid. Profesorul suedez Nils Alwall a încapsulat o versiune modificată a acestui rinichi într-o canistră din oțel inoxidabil, la care s-ar putea aplica o presiune negativă, efectuând astfel prima aplicare cu adevărat practică a hemodializei, care a fost făcută în 1946 la Universitatea din Lund . De asemenea, Alwall a fost, fără îndoială, inventatorul șuntului arteriovenos pentru dializă. El a raportat acest lucru mai întâi în 1948, unde a folosit un astfel de șunt arteriovenos la iepuri. Ulterior, el a folosit astfel de șunturi, realizate din sticlă, precum și dializatorul său închis în canistră, pentru a trata 1500 de pacienți cu insuficiență renală între 1946 și 1960, așa cum a fost raportat Primului Congres Internațional de Nefrologie desfășurat la Evian în septembrie 1960. Alwall a fost numit într-o nouă Catedră de Nefrologie la Universitatea din Lund în 1957. Ulterior, el a colaborat cu omul de afaceri suedez Holger Crafoord pentru a fonda una dintre companiile cheie care vor produce echipamente de dializă în ultimii 50 de ani, Gambro . Istoria timpurie a dializei a fost revizuită de Stanley Shaldon.
Belding H. Scribner , colaborând cu inginerul biomecanic Wayne Quinton , a modificat șunturile de sticlă folosite de Alwall făcându-le din teflon . O altă îmbunătățire cheie a fost conectarea acestora la o bucată scurtă de tubulatură din elastomer de silicon. Aceasta a stat la baza așa-numitului șunt Scribner, poate mai bine numit șunt Quinton-Scribner. După tratament, accesul circulator ar fi menținut deschis prin conectarea celor două tuburi din exteriorul corpului folosind un mic tub de teflon în formă de U, care ar shunta sângele din tubul din arteră înapoi în tubul din venă.
În 1962, Scribner a început prima unitate de dializă ambulatorie din lume, Centrul pentru rinichi artificial din Seattle, redenumit ulterior Centrele pentru rinichi din nord - vest . Imediat a apărut problema cine ar trebui să i se facă dializă, deoarece cererea a depășit cu mult capacitatea celor șase aparate de dializă din centru. Scribner a decis că nu va lua decizia cu privire la cine va primi dializă și cine nu. În schimb, alegerile ar fi făcute de un comitet anonim, care ar putea fi privit ca unul dintre primele comitete de bioetică .
Pentru o istorie detaliată a încercărilor de dializă reușite și nereușite, inclusiv pionieri precum Abel și Roundtree, Haas și Necheles, consultați această recenzie de Kjellstrand.
Vezi si
Referințe
linkuri externe
- Rinichii dvs. și modul în care funcționează - Institutul Național de Diabet și Boli Digestive și Rinichii (american) (NIDDK), NIH .
- Metode de tratament pentru insuficiența renală - (American) Institutul Național de Diabet și Boli Digestive și Renale (NIDDK), NIH .
- Metode de tratament pentru insuficiența renală: hemodializă - (american) Centrul național de informare a bolilor renale și urologice ( NIH) .