Acid cloroplatinic - Chloroplatinic acid
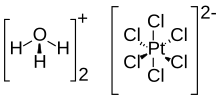
|
|
|
|

|
|
| Numele | |
|---|---|
|
Numele IUPAC
Hexacloroplatinat de dihidroniu (2–)
|
|
| Alte nume
Acid hexacloroplatinic
|
|
| Identificatori | |
|
Model 3D ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.037.267 |
| Numărul CE | |
|
PubChem CID
|
|
| Numărul RTECS | |
| UNII | |
| Numărul ONU | 2507 |
|
Tablou de bord CompTox ( EPA )
|
|
|
|
|
|
| Proprietăți | |
| H 6 Cl 6 O 2 Pt | |
| Masă molară | 409,81 g / mol |
| Aspect | Solid maro roșiatic |
| Densitate | 2,441 g / cm 3 |
| Punct de topire | 60 ° C (140 ° F; 333 K) |
| Punct de fierbere | se descompune |
| foarte solubil | |
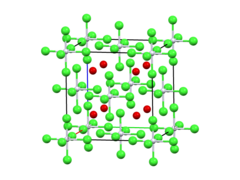
| Structura | |
| Anti-fluorit. | |
| octaedrică | |
| 0 D | |
| Pericole | |
| Fișa cu date de securitate | MSDS extern |
| Pictograme GHS |
   
|
| GHS Cuvânt de avertizare | Pericol |
| H301 , H314 , H317 , H334 | |
| P260 , P261 , P264 , P270 , P272 , P280 , P285 , P301 + 310 , P301 + 330 + 331 , P302 + 352 , P303 + 361 + 353 , P304 + 340 , P304 + 341 , P305 + 351 + 338 , P310 , P321 , P330 , P333 + 313 , P342 + 311 , P363 , P405 , P501 | |
| NFPA 704 (diamant de foc) | |
| Compuși înrudiți | |
|
Alți anioni
|
Acid hexacloropaladic |
|
Alți cationi
|
Hexacloroplatinat de potasiu , hexacloroplatinat de amoniu , hexacloroplatinat de rubidiu, hexacloroplatinat de cesiu |
|
|
|
| Referințe infobox | |
Acidul cloroplatinic (cunoscut și sub numele de acid hexacloroplatinic ) este un compus anorganic cu formula [H 3 O] 2 [PtCl 6 ] (H 2 O) x (0 ≤ x ≤ 6). Un solid roșu, este o sursă comercială importantă de platină , de obicei ca soluție apoasă. Deși este scris adesea pe scurt pe H 2 PtCl 6 , este sarea de hidroniu (H 3 O + ) a anionului hexacloroplatinat ( PtCl2−
6). Acidul hexacloroplatinic este foarte higroscopic .
Producție
Acidul hexacloroplatinic poate fi produs printr-o varietate de metode. Cea mai comună dintre aceste metode implică dizolvarea platinei în aqua regia . Alte metode includ expunerea unei suspensii apoase de particule de platină la clor gazos sau prin electroliză.
Când este produs pe calea aqua regia, se crede că acidul hexacloroplatinic apare prin următoarea ecuație:
- Pt + 4 HNO 3 + 6 HCI → H 2 PtCl 6 + 4 NO 2 + 4 H 2 O
Soluția portocalie / roșie rezultată poate fi evaporată pentru a produce cristale roșii maronii. Unii autori sugerează că acidul hexacloroplatinic produs utilizând această metodă este contaminat cu hexacloroplatinat de nitrozoniu. Literatura mai nouă indică faptul că acest lucru nu este cazul și că odată ce acidul azotic a fost îndepărtat, probele preparate prin această metodă nu conțin azot detectabil.
Au fost investigate și descrise metode alternative, adesea motivate de evitarea contaminării cu azot.
Reacții
Când este încălzit, acidul hexacloroplatinic se descompune în clorură de platină (IV) .
- (H 3 O) 2 PtCl 6 · n H 2 O → PtCl 4 + 2 HCl + ( n + 2) H 2 O
Aplicații
Determinarea potasiului
Acidul cloroplatinic a fost popularizat pentru analiza cantitativă a potasiului. Potasiul este precipitat selectiv din soluție sub formă de hexacloroplatinat de potasiu. Determinările s-au făcut în soluții de alcool 85% (v / v) cu ioni excesivi de platinat și produsul precipitat a fost cântărit. Potasiul poate fi detectat pentru soluții diluate de la 0,02 la 0,2% (m / v).
Această metodă de determinare a potasiului a fost avantajoasă în comparație cu metoda de cobaltinitrit de sodiu utilizată anterior, deoarece a necesitat o singură reacție de precipitare . Analiza gravimetrică a produselor precipitate a fost înlocuită de metode moderne de analiză instrumentală , cum ar fi electrozi selectivi ai ionilor , fotometrie cu flacără , ICP-AES sau ICP-MS .
Purificarea platinei
La tratarea cu o sare de amoniu, cum ar fi clorura de amoniu , acidul cloroplatinic se transformă în hexacloroplatinat de amoniu , care precipită sub formă de solid. La încălzirea într-o atmosferă de hidrogen , sarea de amoniu se transformă în platină elementară. Platina este adesea izolată din minereuri sau reciclată astfel din reziduuri.
Cataliză
La fel ca mulți compuși de platină, acidul cloroplatinic este un catalizator (sau precatalizator) pentru hidrogenare și reacții conexe. Așa cum a fost raportat pentru prima dată de John Speier și colegii de la Dow Corning , acesta catalizează adăugarea de hidrosilani la olefine, adică hidrosililarea . Reacțiile demonstrative timpurii utilizate soluții de izopropanol triclorosilanului (SiHCl 3 ) cu pentene . Lucrările anterioare privind adăugarea silanilor la alchene au necesitat reacții radicale ineficiente. Pe lângă catalizatorul lui Karstedt, catalizatorul lui Speier se bucură de o utilizare pe scară largă pentru hidrosililare, principalul dezavantaj îl reprezintă proprietățile deliquescente ale catalizatorului.
Este în general de acord că acidul cloroplatinic este un precursor al catalizatorului propriu-zis. Un posibil rol pentru platină coloidală sau complexe zero-valente a fost, de asemenea, luat în considerare.
Compuși înrudiți
Se propune ca acidul cloroplatinic preparat din aqua regia să conțină hexacloroplatinat de nitrozoniu, (NO) 2 PtCl 6 . Hexacloroplatinatul de nitrosoniu se obține prin reacția clorurii de nitrozil (NOCl) și a platinei metalice. S-a constatat că hexacloroplatinatul de nitrosoniu reacționează energic cu apa și acidul clorhidric, făcând improbabilă contaminarea acidului cloroplatinic preparat cu aqua regia cu hexacloroplatinat de nitrosoniu.


