Emtricitabină - Emtricitabine
 | |
| Date clinice | |
|---|---|
| Pronunție |
/ ˌ ɛ m t r ə s aɪ t ə b I n / EM -trə- SY -tə-fost |
| Denumiri comerciale | Emtriva |
| Alte nume | FTC |
| AHFS / Drugs.com | Monografie |
| MedlinePlus | a604004 |
| Date despre licență | |
Categoria sarcinii |
|
| Căi de administrare |
Prin gura |
| Codul ATC | |
| Statut juridic | |
| Statut juridic | |
| Date farmacocinetice | |
| Biodisponibilitate | 93% |
| Legarea proteinelor | Foarte scăzut (mai puțin de 4%) |
| Metabolism |
Sistemul CYP de oxidare și glucuronidare hepatică nu este implicat |
| Timp de înjumătățire prin eliminare | 10 ore |
| Excreţie | Renale (86%) și fecale (14%) |
| Identificatori | |
| |
| Numar CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| NIAID ChemDB | |
| CompTox Dashboard ( EPA ) | |
| ECHA InfoCard |
100.120.945 |
| Date chimice și fizice | |
| Formulă | C 8 H 10 F N 3 O 3 S |
| Masă molară | 247,24 g · mol −1 |
| Model 3D ( JSmol ) | |
| |
| |
| (verifica) | |
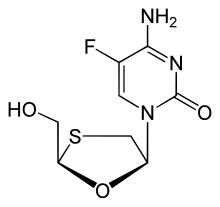
Emtricitabina (denumită în mod obișnuit FTC , denumire sistematică 2 ', 3'-dideoxi-5-fluor-3'-tiacitidină), cu denumirea comercială Emtriva (anterior Coviracil ), este un inhibitor al nucleozidelor revers-transcriptazei (NRTI) pentru prevenirea și tratamentul a infecției cu HIV la adulți și copii.
Emtricitabina este, de asemenea, comercializată într-o combinație cu doză fixă cu tenofovir disoproxil (Viread) sub numele Truvada și cu tenofovir alafenamidă (Vemlidy) sub numele Descovy.
O combinație triplă cu doză fixă de emtricitabină, tenofovir și efavirenz (Sustiva, comercializată de Bristol-Myers Squibb ) a fost aprobată de Administrația SUA pentru Alimente și Medicamente (FDA) la 12 iulie 2006, sub numele de marcă Atripla .
Emtricitabina reprezintă o pătrime din pastila Quad (nume de marcă: Stribild și Genvoya).
În combinații cu doze fixe cu tenofovir sau cu efavirenz și tenofovir, acesta se află pe lista medicamentelor esențiale a Organizației Mondiale a Sănătății . În 2017, acesta a fost al 224-lea medicament cel mai frecvent prescris în Statele Unite, cu peste două milioane de rețete.
Utilizări medicale
Infecția cu HIV
Emtricitabina este indicată în asociere cu alți agenți antiretrovirali pentru prevenirea și tratamentul infecției cu HIV-1.
Infecția cu VHB
Emtricitabina prezintă activitate clinică împotriva virusului hepatitei B (VHB), dar nu este aprobată de Administrația SUA pentru Alimente și Medicamente (FDA) pentru tratamentul infecției cu VHB. Dintre persoanele cu infecție cronică cu VHB, tratamentul cu emtricitabină are ca rezultat îmbunătățiri semnificative histologice, virologice și biochimice. Profilul de siguranță al emtricitabinei în timpul tratamentului este similar cu cel al unui placebo. Emtricitabina, ca toate celelalte medicamente aprobate de FDA, nu vindecă nici infecția cu HIV, nici cu VHB. Într-un studiu care a implicat persoane cu infecție cu VHB, simptomele infecției au revenit la 23% dintre persoanele tratate cu emtricitabină care au fost eliminate de la tratament. În studiile care implică persoane cu infecție cronică cu HIV, replicarea virală se reia și atunci când subiecții studiați sunt eliminați din terapie. Ca și în cazul medicamentelor utilizate pentru tratarea infecției cu HIV, medicamentele utilizate pentru tratarea infecției cu VHB pot fi utilizate în combinație pentru a preveni evoluția tulpinilor rezistente la medicamente. Eficacitatea emtricitabinei în combinație cu alte medicamente anti-VHB nu a fost stabilită.
Efecte secundare
În practica clinică, toxicitatea cu emtricitabină este neobișnuită. Cele mai frecvente evenimente adverse legate de tratament sunt diareea , cefaleea , greața și erupția cutanată . Aceste simptome sunt în general ușoare până la moderate ca severitate, dar au determinat 1% dintre pacienții din studiile clinice să renunțe la tratament. Decolorarea pielii, care este de obicei raportată ca hiperpigmentare și care afectează de obicei fie palmele mâinilor, fie tălpile picioarelor, este raportată la mai puțin de 2% dintre indivizi și este aproape exclusivă pacienților de origine africană .
Printre cele mai severe reacții adverse pe care le pot prezenta pacienții se numără hepatotoxicitatea sau o acidoză lactică .
Mecanism de acțiune
Emtricitabina este un analog al citidinei . Medicamentul funcționează prin inhibarea transcriptazei inverse , enzima care copiază ARN-ul HIV într-un nou ADN viral. Prin interferența cu acest proces, care este esențial pentru replicarea HIV, emtricitabina poate ajuta la scăderea cantității de HIV, sau „ încărcătura virală ”, în corpul pacientului și poate crește indirect numărul de celule ale sistemului imunitar (și anume celulele T / Celule T CD4 + ). Ambele modificări sunt asociate cu sisteme imune mai sănătoase și cu o probabilitate redusă de boli grave.
Istorie
Emtricitabina a fost descoperită de Dr. Dennis C. Liotta , Dr. Raymond F. Schinazi și Dr. Woo-Baeg Choi de la Universitatea Emory și licențiată la Triangle Pharmaceuticals de Emory în 1996. Triangle Pharmaceuticals a fost achiziționată în 2003 de Gilead Sciences , care a finalizat dezvoltarea și comercializarea produsului cu numele Emtriva.
A fost aprobat de FDA 2 iulie 2003. Este foarte asemănător cu lamivudina (3TC), iar rezistența încrucișată între cele două este aproape universală.
Referințe
linkuri externe
- „Emtricitabină” . Portalul de informații despre droguri . Biblioteca Națională de Medicină din SUA.
