Legătură glicozidică - Glycosidic bond
O legătură glicozidică sau legătură glicozidică este un tip de legătură covalentă care unește o moleculă de carbohidrați (zahăr) cu un alt grup, care poate fi sau nu un alt carbohidrat.
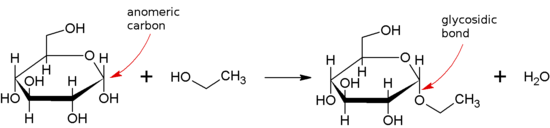
O legătură glicozidică se formează între grupul hemiacetal sau hemicetal al unei zaharide (sau o moleculă derivată dintr-o zaharidă) și gruparea hidroxilă a unor compuși precum un alcool . O substanță care conține o legătură glicozidică este o glicozidă .
Termenul „glicozidă” este acum extins pentru a acoperi și compușii cu legături formate între grupuri hemiacetale (sau hemicetale) de zaharuri și mai multe grupuri chimice, altele decât hidroxilii, cum ar fi -SR (tioglicozide), -SeR (selenoglicozide), -NR 1 R 2 (N-glicozide) sau chiar -CR 1 R 2 R 3 (C-glicozide).
În special în glicozidele naturale, compusul ROH din care a fost îndepărtat reziduul de carbohidrați este adesea denumit aglicona, iar reziduul de carbohidrat în sine este uneori denumit „glicona”.
Legături S-, N-, C- și O-glicozidice
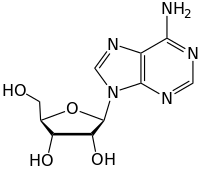
Legăturile glicozidice de forma discutată mai sus sunt cunoscute sub numele de legături O-glicozidice , cu referire la oxigenul glicozidic care leagă glicozida de agliconă sau zahărul final reducător. În analogie, se iau în considerare și legăturile S-glicozidice (care formează tioglicozide ), unde oxigenul legăturii glicozidice este înlocuit cu un atom de sulf . În același mod, legăturile N-glicozidice , au legătura glicozidică oxigen înlocuită cu azot . Substanțele care conțin legături N-glicozidice sunt cunoscute și sub numele de glicozilamine . Legăturile C-glicozil au oxigenul glicozidic înlocuit cu un carbon ; termenul "glicozid C" este considerat un nume incorect de IUPAC și este descurajat. Toate aceste legături glicozidice modificate au susceptibilitate diferită la hidroliză și, în cazul structurilor C-glicozil, sunt de obicei mai rezistente la hidroliză.
Numerotarea și distincția α / β a legăturilor glicozidice
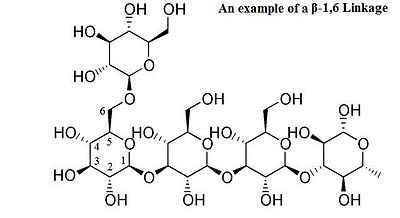
Când un centru anomeric este implicat într-o legătură glicozidică (așa cum este obișnuit în natură), atunci se poate distinge între legăturile α- și β-glicozidice prin stereochimia relativă a poziției anomerice și stereocentrul cel mai îndepărtat de C1 în zaharidă.
Farmacologii adesea îmbină substanțele cu acidul glucuronic prin legături glicozidice pentru a le crește solubilitatea în apă ; aceasta este cunoscută sub numele de glucuronidare . Multe alte glicozide au funcții fiziologice importante.
Abordări chimice
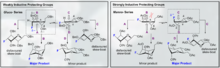
Nüchter și colab. (2001) au arătat o nouă abordare a glicozidării Fischer . Utilizarea unui cuptor cu microunde echipat cu aparat de reflux într-un reactor cu rotor cu bombe de presiune , Nüchter și colab. (2001) au reușit să obțină un randament de 100% de α- și β-D-glucozide. Această metodă poate fi realizată pe o scară de mai multe kilograme.
- Metoda lui Vishal Y Joshi
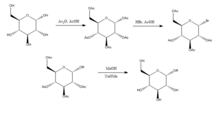
Joshi și colab. (2006) propun metoda Koenigs-Knorr în sinteza stereoselectivă a alchil D-glucopiranozidelor prin glicozilare, cu excepția utilizării carbonatului de litiu care este mai puțin costisitor și toxic decât metoda convențională de utilizare a sărurilor de argint sau mercur . D-glucoza este mai întâi protejată prin formarea peracetatului prin adăugarea de anhidridă acetică în acid acetic și apoi prin adăugarea de bromură de hidrogen care se bromează în poziția 5. La adăugarea alcoolului ROH și a carbonatului de litiu, OR înlocuiește bromul și la deprotejarea hidroxililor acetilați, produsul este sintetizat cu o puritate relativ ridicată. A fost sugerat de Joshi și colab. (2001) că litiul acționează ca nucleofil care atacă carbonul în poziția 5 și printr-o stare de tranziție alcoolul este substituit grupului brom. Avantajele acestei metode, precum și stereoselectivitatea și costul redus al sării de litiu includ faptul că se poate face la temperatura camerei și randamentul său se compară relativ bine cu metoda convențională Koenigs-Knorr.
Hidrolaze glicozidice
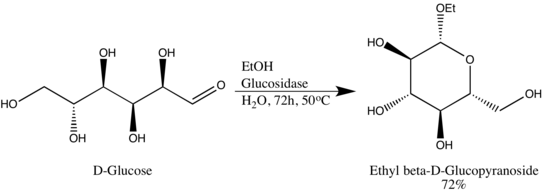
Glicozidele hidrolaze (sau glicozidazele), sunt enzime care rup legăturile glicozidice. Hidrolazele glicozidice pot acționa de obicei fie asupra legăturilor α-, fie asupra legăturilor β-glicozidice, dar nu asupra ambelor. Această specificitate permite cercetătorilor să obțină glicozide în exces epimeric ridicat, un exemplu fiind conversia lui Wen-Ya Lu a D-Glucozei în Etil β-D-glucopiranozid folosind glucozidază derivată în mod natural. Este demn de remarcat faptul că Wen-Ya Lu a utilizat glucozidaza într-un mod invers opus funcționalității biologice a enzimei:
Glicoziltransferaze
Înainte ca unitățile de monozaharide să fie încorporate în glicoproteine, polizaharide sau lipide în organismele vii, ele sunt de obicei „activate” prin a fi unite printr-o legătură glicozidică la gruparea fosfat a unui nucleotid, cum ar fi uridina difosfat (UDP), guanosina difosfat (PIB) , difosfat de timidină (TDP) sau monofosfat de citidină (CMP). Acești intermediari biochimici activi sunt cunoscuți ca nucleotide de zahăr sau donatori de zahăr. Multe căi biosintetice utilizează mono- sau oligozaharide activate de o legătură difosfatică cu lipide, cum ar fi dolichol . Acești donatori activi sunt apoi substraturi pentru enzime cunoscute sub numele de glicoziltransferaze , care transferă unitatea de zahăr de la donatorul activat la un nucleofil acceptant (substratul acceptor).
Fosforilazele dizaharidice
S-au dezvoltat diferite abordări biocatalitice spre sinteza glicozidelor în ultimele decenii, care folosind „glicoziltransferaze” și „glicozide hidrolaze” sunt printre cele mai frecvente catalize. Primul are adesea nevoie de materiale scumpe, iar cel din urmă prezintă deseori randamente scăzute, De Winter și colab. investigarea utilizării celobiozei fosforilazei (CP) spre sinteza alfa-glicozidelor în lichide ionice. Cea mai bună condiție pentru utilizarea CP a fost găsită în prezența IL AMMOENG 101 și acetat de etil.
Glicozilări direcționate
Există mai multe abordări chimice pentru a încuraja selectivitatea legăturilor α- și β-glicozidice. Natura deosebit de specifică substratului selectivității și activitatea generală a piranozidei poate oferi dificultăți majore de sinteză. Specificitatea generală a glicozilării poate fi îmbunătățită prin utilizarea abordărilor care iau în considerare stările relative de tranziție pe care le poate suferi carbonul anomeric în timpul unei glicozilări tipice. În special, recunoașterea și încorporarea modelelor Felkin-Ahn-Eisenstein în raționamentul proiectării chimice poate oferi în general rezultate fiabile, cu condiția ca transformarea să poată fi supusă acestui tip de control conformațional în starea de tranziție.
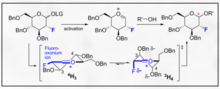
Glicozilările direcționate de fluor reprezintă o manieră încurajatoare atât pentru selectivitatea B, cât și pentru introducerea unei funcționalități C2 biomimetice nenaturale pe carbohidrați. Un exemplu inovator furnizat de Bucher și colab. oferă o modalitate de a utiliza un ion fluor oxoniu și tricloracetimidatul pentru a încuraja stereoselectivitatea B prin intermediul efectului gauche. Această stereoselectivitate rezonabilă este clară prin vizualizarea modelelor Felkin-Ahn ale posibilelor forme de scaune.
Această metodă reprezintă o modalitate încurajatoare de selectivitate de a încorpora B-etil, izopropil și alte glicozide cu chimie tipică tricloracetimidatului.
Glicopeptide legate de O; utilizări farmaceutice ale peptidelor O-glicozilate
Glicopeptidele legate de O s-au arătat recent că prezintă o permeabilitate și o eficacitate SNC excelente în mai multe modele animale cu stări de boală. În plus, unul dintre cele mai interesante aspecte ale acesteia este capacitatea O-glicozilării de a prelungi timpul de înjumătățire, de a reduce clearance-ul și de a îmbunătăți PK / PD al acestuia, peptida activă dincolo de creșterea penetrării SNC. Utilizarea înnăscută a zaharurilor ca porțiuni de solubilizare în metabolismul de fază II și III (acizi glucuronic) a permis remarcabil un avantaj evolutiv prin faptul că enzimele mamiferelor nu sunt direct dezvoltate pentru a degrada produsele glicozilate O pe porțiuni mai mari.
Natura particulară a glicopeptidelor legate de O este că există numeroase exemple care sunt penetrante ale SNC. Se crede că baza fundamentală a acestui efect implică „saltarea membranei” sau „difuziunea hameiului”. Se consideră că procesul de „difuzie a hameiului” condus de mișcare non-browniană se produce din cauza discontinuității membranei plasmatice. „Difuziunea hameiului” combină în special difuzia liberă și tranzițiile intercomparmentale. Exemple recente includ în special permeabilitatea ridicată a analogilor met-encefalină printre alte peptide. Pentapeptida agonistă MOR completă DAMGO este, de asemenea, penetrantă a SNC la introducerea glicozilării.
Referințe
- Marco Brito-Arias, „Sinteza și caracterizarea glicozidelor”, ediția a doua, Editorial Springer 2016.
linkuri externe
- Definiția glicozidelor , din Compendiul IUPAC de terminologie chimică, „ Cartea de aur ”
- Varki A și colab. Elementele esențiale ale glicobiologiei. Presa de laborator Cold Spring Harbor; 1999. Căutare online