Epilepsie posttraumatică - Post-traumatic epilepsy
| Epilepsie posttraumatică | |
|---|---|
| Specialitate | Neurologie |
Epilepsia post-traumatică ( PTE ) este o formă de epilepsie dobândită care rezultă din leziuni cerebrale cauzate de traume fizice la nivelul creierului ( leziuni cerebrale traumatice , abreviat TBI). O persoană cu PTE suferă crize post-traumatice repetate (PTS, convulsii care rezultă din TBI) la mai mult de o săptămână după leziunea inițială. PTE se estimează că reprezintă 5% din toate cazurile de epilepsie și peste 20% din cazurile de epilepsie dobândită (în care convulsiile sunt cauzate de o afecțiune organică identificabilă a creierului).
Nu se știe cum se prezice cine va dezvolta epilepsie după TBI și cine nu. Cu toate acestea, probabilitatea ca o persoană să dezvolte TEP este influențată de gravitatea și tipul de leziune; de exemplu leziunile penetrante și cele care implică sângerări în creier conferă un risc mai mare. Debutul PTE poate apărea într-un timp scurt de la trauma fizică care o provoacă, sau luni sau ani după aceea. Persoanele cu traumatism cranian pot rămâne la un risc mai mare de convulsii post-traumatice decât populația generală chiar și la decenii după leziune. PTE poate fi cauzată de mai multe procese biochimice care apar în creier după traume, inclusiv supraexcitația celulelor creierului și deteriorarea țesuturilor cerebrale de către radicalii liberi .
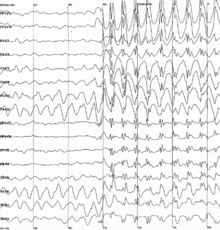
Măsurile de diagnostic includ electroencefalografia (EEG) și tehnici de imagistică a creierului, cum ar fi imagistica prin rezonanță magnetică , dar acestea nu sunt total fiabile. Medicamentele antiepileptice nu împiedică dezvoltarea PTE după leziuni la nivelul capului, dar pot fi utilizate pentru tratarea afecțiunii dacă apare. Când medicamentele nu funcționează pentru a controla convulsiile, poate fi necesară o intervenție chirurgicală. Tehnicile chirurgicale moderne pentru PTE își au rădăcinile în secolul al XIX-lea, dar trepanarea (tăierea unei găuri în craniu) poate fi folosită pentru această afecțiune în culturile antice.
Clasificare
Convulsiile pot apărea după leziuni traumatice ale creierului; acestea sunt cunoscute sub numele de convulsii posttraumatice (PTS). Cu toate acestea, nu toți cei care au crize post-traumatice vor continua să aibă epilepsie post-traumatică, deoarece aceasta din urmă este o afecțiune cronică. Cu toate acestea, termenii PTS și PTE sunt folosiți în mod alternativ în literatura medicală. Convulsiile datorate epilepsiei post-traumatice sunt diferențiate de convulsiile post-traumatice neepileptice în funcție de cauza și momentul lor după traumatism. O persoană cu TEP suferă crize tardive, cele care apar la mai mult de o săptămână după trauma inițială. Convulsiile tardive sunt considerate a fi neprovocate, în timp ce convulsiile timpurii (cele care apar în decurs de o săptămână de la traume) sunt considerate a rezulta din efectele directe ale leziunii. O criză provocată este cea care rezultă dintr-o cauză excepțională, care nu se repetă, cum ar fi efectele imediate ale traumei, mai degrabă decât un defect al creierului; nu este o indicație a epilepsiei. Astfel, pentru un diagnostic de PTE, convulsiile trebuie să nu fie provocate.
Există dezacord cu privire la definirea PTE ca la apariția uneia sau mai multor convulsii tardive, neprovocate sau dacă starea ar trebui diagnosticată numai la persoanele cu două sau mai multe. Sursele medicale consideră că PTE este prezentă dacă apare chiar și o criză neprovocată, dar mai recent a devenit acceptată restricționarea definiției tuturor tipurilor de epilepsie pentru a include doar condiții în care apar mai multe. Necesitarea mai multor crize pentru diagnosticarea PTE este în concordanță cu definiția modernă a epilepsiei, dar elimină persoanele pentru care convulsiile sunt controlate de medicamente după prima criză.
Ca și în cazul altor forme de epilepsie, tipurile de convulsii în PTE pot fi parțiale (afectând doar o parte a unei emisfere ale creierului) sau generalizate (afectând ambele emisfere și asociate cu pierderea cunoștinței). În aproximativ o treime din cazuri, persoanele cu TEP au convulsii parțiale; acestea pot fi simple sau complexe. În convulsiile parțiale simple, nivelul conștiinței nu este modificat, în timp ce în convulsiile parțiale complexe conștiința este afectată. Când apar crize generalizate, acestea pot începe ca crize parțiale și apoi se pot răspândi pentru a deveni generalizate.
Cauze
Nu este clar de ce unii pacienți dezvoltă TEP, în timp ce alții cu leziuni foarte similare nu. Cu toate acestea, au fost identificați posibili factori de risc, inclusiv gravitatea și tipul de leziune, prezența convulsiilor timpurii și factorii genetici.
Genetica
Genetica poate juca un rol în riscul ca o persoană să dezvolte TEP; persoanele cu alela ApoE-ε4 pot prezenta un risc mai mare de PTE. Haptoglobina HP2-2 Alela poate fi un alt factor de risc genetic, eventual , pentru ca se leaga de hemoglobina slab și permite astfel mai mult fier să scape și țesuturi daune. Cu toate acestea, majoritatea studiilor au constatat că a avea membri ai familiei cu epilepsie nu crește semnificativ riscul de STP, sugerând că genetica nu este un factor de risc puternic.
Severitatea traumei
Cu cât trauma cerebrală este mai severă, cu atât este mai probabil ca o persoană să sufere PTE tardivă. Dovezile sugerează că leziunile ușoare ale capului nu conferă un risc crescut de apariție a TEP, în timp ce tipurile mai severe. În TBI ușoară simplă, riscul pentru TEP este de aproximativ 1,5 ori mai mare decât al populației nevătămate. După unele estimări, până la jumătate dintre cei care suferă de traumatisme cerebrale severe suferă de TEP; alte estimări plasează riscul la 5% pentru toți pacienții cu TBI și 15-20% pentru TBI severă. Un studiu a constatat că riscul de 30 de ani de a dezvolta PTE a fost de 2,1% pentru TBI ușor, 4,2% pentru moderat și 16,7% pentru leziuni grave, după cum se arată în graficul din dreapta.
Natura traumei
Natura traumatismului cranian influențează, de asemenea, riscul de TEP. Persoanele care suferă de fracturi de craniu deprimate , traumatisme penetrante ale capului , PTS precoce și hematoame intracerebrale și subdurale cauzate de TBI sunt susceptibile în special să sufere de TEP, care apare la mai mult de 30% dintre persoanele cu oricare dintre aceste constatări. Aproximativ 50% dintre pacienții cu traumatism cranian penetrant dezvoltă TEP, iar leziunile rachetelor și pierderea volumului creierului sunt asociate cu o probabilitate deosebit de mare de a dezvolta afecțiunea. Leziunile care apar în medii militare prezintă un risc mai mare decât cel obișnuit pentru PTE, probabil deoarece implică mai frecvent leziuni cerebrale penetrante și leziuni cerebrale într-o zonă mai răspândită. Hematoamele intracraniene , în care sângele se acumulează în interiorul craniului, sunt unul dintre cei mai importanți factori de risc pentru TEP. Hematomul subdural conferă un risc mai mare de TEP decât hematomul epidural, posibil deoarece cauzează mai multe leziuni ale țesutului cerebral. Chirurgia intracraniană repetată conferă un risc ridicat de TEP târziu, posibil deoarece persoanele care au nevoie de mai multe intervenții chirurgicale au mai multe șanse să aibă factori asociați cu traume cerebrale mai grave, cum ar fi hematoame mari sau umflături cerebrale . În plus, șansele de a dezvolta PTE diferă în funcție de localizarea leziunii cerebrale: contuzia creierului care apare într-unul sau altul din lobii frontali prezintă un risc de 20% PTE, în timp ce o contuzie în unul dintre parietale lobii prezintă un risc de 19%, iar unul dintr-un lob temporal are o șansă de 16%. Când apar contuzii în ambele emisfere, riscul este de 26% pentru lobii frontali, 66% pentru parietal și 31% pentru temporal.
Convulsii posttraumatice
Riscul ca o persoană să dezvolte PTE este crescut, dar nu 100% dacă apar PTS. Deoarece mulți dintre factorii de risc atât pentru PTE cât și pentru PTS timpuriu sunt aceiași, nu se știe dacă apariția PTS este un factor de risc în sine. Cu toate acestea, chiar și independent de alți factori de risc comuni, s-a constatat că PTS timpuriu crește riscul de PTE la peste 25% în majoritatea studiilor. O persoană care are o criză târzie are un risc și mai mare de a avea o altă persoană decât una care are TSP precoce; epilepsia apare la 80% dintre persoanele care au o convulsie tardivă. Starea epileptică , o criză continuă sau crize multiple în succesiune rapidă, este corelată în special puternic cu dezvoltarea PTE; convulsiile de stare apar la 6% din toate TBI, dar sunt asociate cu PTE 42% din timp, iar oprirea rapidă a unei convulsii de stare reduce șansele de dezvoltare a PTE.
Fiziopatologie
Din motive necunoscute, trauma poate provoca modificări ale creierului care duc la epilepsie. Există o serie de mecanisme propuse prin care TBI provoacă PTE, dintre care mai multe pot fi prezente la o persoană dată. În perioada dintre o leziune cerebrală și debutul epilepsiei, celulele creierului pot forma sinapse și axoni noi , pot suferi apoptoză sau necroză și pot experimenta modificarea expresiei genice . În plus, deteriorarea zonelor deosebit de vulnerabile ale cortexului, cum ar fi hipocampusul, poate da naștere PTE.
Sângele care se adună în creier după o leziune poate deteriora țesutul cerebral și, prin urmare, poate provoca epilepsie. Produsele care rezultă din descompunerea hemoglobinei din sânge pot fi toxice pentru țesutul cerebral. „Ipoteza fierului” susține că PTE se datorează deteriorării radicalilor liberi de oxigen , a căror formare este catalizată de fierul din sânge. Experimentele pe animale folosind șobolani au arătat că convulsiile epileptice pot fi produse prin injectarea de fier în creier. Fierul catalizează formarea radicalilor hidroxil prin reacția Haber-Weiss ; astfel de radicali liberi afectează celulele creierului prin peroxidarea lipidelor din membranele lor . Fierul din sânge reduce, de asemenea, activitatea unei enzime numită oxid nitric sintază , un alt factor despre care se crede că contribuie la PTE.
După TBI, există anomalii în eliberarea neurotransmițătorilor , substanțe chimice utilizate de celulele creierului pentru a comunica între ele; aceste anomalii pot juca un rol în dezvoltarea PTE. TBI poate duce la eliberarea excesivă a glutamatului și a altor neurotransmițători excitatori (cei care stimulează celulele creierului și cresc probabilitatea ca acestea să se declanșeze ). Această eliberare excesivă de glutamat poate duce la excitotoxicitate , deteriorarea celulelor creierului prin supraactivarea receptorilor biochimici care se leagă și răspund la neurotransmițătorii excitatori. Supraactivarea receptorilor de glutamat dăunează neuronilor; de exemplu duce la formarea radicalilor liberi. Excitotoxicitatea este un posibil factor în dezvoltarea PTE; poate duce la formarea unui focar epileptogen cronic. Un focar epileptic este partea creierului din care provin descărcările epileptice.
Pe lângă modificările chimice ale celulelor, în creier pot apărea modificări structurale care duc la epilepsie. Convulsiile care apar la scurt timp după TBI pot reorganiza rețelele neuronale și pot provoca convulsii în mod repetat și spontan mai târziu. Ipoteza surcele sugereaza ca noi conexiuni neuronale sunt formate in creier si determina o crestere a excitabilitate. Cuvântul aprindere este o metaforă: modul în care creșterea răspunsului creierului la stimuli crește în urma expunerilor repetate este similar cu modul în care crenguțele mici arzătoare pot produce un foc mare. Această reorganizare a rețelelor neuronale le poate face mai excitabile. Neuronii care se află într-o stare hiperexcitabilă din cauza traumei pot crea un focar epileptic în creier care duce la convulsii. În plus, o creștere a excitabilității neuronilor poate însoți pierderea neuronilor inhibitori care servesc în mod normal la reducerea probabilității ca alți neuroni să se declanșeze; aceste modificări pot produce, de asemenea, PTE.
Diagnostic
Pentru a fi diagnosticată cu PTE, o persoană trebuie să aibă antecedente de traumatisme craniene și nici antecedente de convulsii înainte de vătămare. Asistarea la o criză este cel mai eficient mod de a diagnostica PTE. Electroencefalografia (EEG) este un instrument utilizat pentru diagnosticarea unei tulburări convulsive, dar o mare parte din persoanele cu PTE ar putea să nu aibă descoperirile EEG "epileptiforme" anormale care indică epilepsie. Într-un studiu, aproximativ o cincime din persoanele care aveau EEG normale la trei luni după o leziune au dezvoltat ulterior PTE. Cu toate acestea, deși EEG nu este util pentru a prezice cine va dezvolta PTE, poate fi util să localizați focalizarea epileptică, să determinați severitatea și să prevedeți dacă o persoană va suferi mai multe convulsii dacă încetează să ia medicamente antiepileptice.
Imagistica prin rezonanță magnetică (RMN) este efectuată la persoanele cu PTE, iar scanarea CT poate fi utilizată pentru a detecta leziunile cerebrale dacă RMN-ul nu este disponibil. Cu toate acestea, frecvent nu este posibil să se detecteze focalizarea epileptică folosind neuroimagistica .
Pentru un diagnostic de TEP, convulsiile nu trebuie să fie atribuite unei alte cauze evidente. Convulsiile care apar după rănirea capului nu se datorează neapărat epilepsiei sau chiar traumei capului. La fel ca oricine altcineva, supraviețuitorii TBI pot suferi convulsii din cauza unor factori precum dezechilibre de lichide sau electroliți , epilepsie din alte cauze, hipoxie (oxigen insuficient) și ischemie (flux insuficient de sânge în creier). Retragerea din alcool este o altă cauză potențială a convulsiilor. Astfel, acești factori trebuie excluși ca fiind cauze ale convulsiilor la persoanele cu leziuni ale capului înainte de a putea fi pus un diagnostic de PTE.
Prevenirea
Prevenirea PTE implică prevenirea traumei cerebrale în general; măsurile de protecție includ căști de biciclete și scaune de siguranță pentru copii. Nu există tratament specific pentru a preveni dezvoltarea epilepsiei după apariția TBI. În trecut, medicamentele antiepileptice erau utilizate cu intenția de a preveni dezvoltarea PTE. Cu toate acestea, în timp ce medicamentele antiepileptice pot preveni PTS precoce , studiile clinice nu au reușit să demonstreze că utilizarea profilactică a medicamentelor antiepileptice împiedică dezvoltarea PTE. De ce medicamentele antiepileptice din studiile clinice nu au reușit să oprească dezvoltarea TEP nu este clar, dar au fost oferite mai multe explicații. Este posibil ca medicamentele să nu fie capabile să prevină epilepsia sau studiile cu medicamente ar fi putut fi create într-un mod care să nu permită găsirea unui beneficiu al medicamentelor (de exemplu, medicamentele pot fi administrate prea târziu sau în doze inadecvate). În mod similar, studiile la animale nu au reușit să arate un efect protector al celor mai frecvent utilizate medicamente pentru convulsii în studiile PTE, cum ar fi fenitoina și carbamazepina . Medicamentele antiepileptice sunt recomandate pentru a preveni convulsiile tardive numai pentru persoanele la care PTE a fost deja diagnosticat, nu ca măsură preventivă. Pe baza studiilor menționate mai sus, niciun tratament nu este acceptat pe scară largă pentru a preveni dezvoltarea epilepsiei. Cu toate acestea, s-a propus că poate exista o fereastră îngustă de aproximativ o oră după TBI, timp în care administrarea de antiepileptice ar putea preveni epileptogeneza (dezvoltarea epilepsiei).
Corticosteroizii au fost, de asemenea, investigați pentru prevenirea PTE, dar studiile clinice au arătat că medicamentele nu au redus PTS târziu și au fost de fapt legate de o creștere a numărului de PTS timpurii.
Tratament
Se pot administra medicamente antiepileptice pentru a preveni convulsiile ulterioare; aceste medicamente elimină complet convulsiile pentru aproximativ 35% dintre persoanele cu PTE. Cu toate acestea, antiepilepticele previn convulsiile numai în timp ce sunt luate; acestea nu reduc apariția odată ce pacientul încetează să mai ia medicamentele. Medicamentul poate fi oprit după ce convulsiile au fost controlate timp de doi ani. PTE este de obicei dificil de tratat cu terapia medicamentoasă, iar medicamentele antiepileptice pot fi asociate cu efecte secundare . Medicamentele antiepileptice carbamazepina și valproatul sunt cele mai frecvente medicamente utilizate pentru tratamentul TEP; fenitoina poate fi, de asemenea, utilizată, dar poate crește riscul de efecte secundare cognitive, cum ar fi tulburarea de gândire. Alte medicamente utilizate în mod obișnuit pentru tratamentul PTE includ clonazepam , fenobarbitol , primidonă , gabapentină și etosuximidă . Dintre medicamentele antiepileptice testate pentru prevenirea convulsiilor după TBI (fenitoină, valproat de sodiu, carbamazepină, fenobarbital), nicio dovadă din studiile controlate randomizate nu a arătat superioritatea una față de alta.
Persoanele al căror PTE nu răspunde la medicamente pot fi supuse unei intervenții chirurgicale pentru a elimina focalizarea epileptogenă, partea creierului care provoacă convulsiile. Cu toate acestea, intervenția chirurgicală pentru PTE poate fi mai dificilă decât pentru epilepsie din alte cauze și este mai puțin probabil să fie utilă în PTE decât în alte forme de epilepsie. Poate fi deosebit de dificil în PTE să localizeze focalizarea epileptică, în parte deoarece TBI poate afecta zonele difuze ale creierului. Dificultatea de localizare a focarului convulsivant este văzută ca un factor de descurajare a intervenției chirurgicale. Cu toate acestea, pentru persoanele cu scleroză din lobul temporal mezial (în aspectul interior al lobului temporal), care cuprind aproximativ o treime din persoanele cu PTE intratabil, intervenția chirurgicală va avea probabil un rezultat bun. Atunci când există focare epileptice multiple sau focalizarea nu poate fi localizată, iar terapia medicamentoasă nu este eficientă, stimularea nervului vag este o altă opțiune pentru tratarea TEP.
Persoanele cu TEP au vizite de urmărire, în care furnizorii de servicii medicale monitorizează funcția neurologică și neuropsihologică și evaluează eficacitatea și efectele secundare ale medicamentelor. La fel ca în cazul celor care suferă de alte tipuri de epilepsie, persoanelor care suferă de TEP li se recomandă să fie prudenți atunci când efectuează activități pentru care convulsiile ar putea fi deosebit de riscante, cum ar fi alpinismul.
Prognoză
Prognosticul pentru epilepsie datorată traumei este mai rău decât cel pentru epilepsie cu cauză nedeterminată. Se crede că persoanele cu TEP au speranțe de viață mai scurte decât persoanele cu leziuni cerebrale care nu suferă de convulsii. În comparație cu persoanele cu leziuni cerebrale structurale similare, dar fără PTE, persoanele cu PTE iau mai mult timp pentru a se recupera de la leziune, au mai multe probleme cognitive și motorii și se comportă mai prost la sarcinile de zi cu zi. Această constatare poate sugera că PTE este un indicator al unei leziuni cerebrale mai severe, mai degrabă decât o complicație care în sine înrăutățește rezultatul. De asemenea, s-a constatat că PTE este asociat cu rezultate sociale și funcționale mai proaste, dar nu agravează reabilitarea pacienților sau capacitatea de a reveni la muncă. Cu toate acestea, persoanele cu TEP pot avea probleme în găsirea unui loc de muncă dacă recunosc că au crize, mai ales dacă munca lor implică exploatarea utilajelor grele.
Perioada de timp dintre o leziune și dezvoltarea epilepsiei variază și nu este neobișnuit ca o leziune să fie urmată de o perioadă latentă fără crize recurente. Cu cât o persoană trece mai mult fără a dezvolta convulsii, cu atât sunt mai mici șansele ca epilepsia să se dezvolte. Cel puțin 80-90% dintre persoanele cu TEP au prima criză în termen de doi ani de la TBI. Persoanele fără crize convulsive în termen de trei ani de la accidentare au doar șanse de 5% să dezvolte epilepsie. Cu toate acestea, un studiu a constatat că supraviețuitorii traumatismelor craniene prezintă un risc crescut de PTE până la 10 ani după TBI moderat și peste 20 de ani după TBI sever. Deoarece trauma capului este destul de frecventă și epilepsia poate apărea târziu după leziune, poate fi dificil să se stabilească dacă un caz de epilepsie a rezultat în urma traumei capului în trecut sau dacă trauma a fost incidentală.
Întrebarea privind cât timp o persoană cu PTE rămâne la un risc mai mare de convulsii decât populația generală este controversată. Aproximativ jumătate din cazurile PTE intră în remisie , dar cazurile care apar mai târziu pot avea șanse mai mici de a face acest lucru.
Epidemiologie
Studiile au descoperit că incidența PTE variază între 1,9 și mai mult de 30% din persoanele care suferă de TBI, variind în funcție de gravitatea leziunii și de perioada de timp după TBI pentru care studiile au urmat subiecții.
Trauma cerebrală este unul dintre cei mai puternici factori predispozanți pentru dezvoltarea epilepsiei și este un factor deosebit de important la adulții tineri. Adulții tineri, care prezintă cel mai mare risc de leziuni ale capului , au, de asemenea, cea mai mare rată de TEP, care este cea mai mare cauză a cazurilor de epilepsie cu debut nou la tineri. Copiii au un risc mai mic de a dezvolta epilepsie; 10% dintre copiii cu TBI severă și 16-20% dintre adulții răniți în mod similar dezvoltă TEP. A fi mai mare de 65 de ani este, de asemenea, un factor predictiv în dezvoltarea epilepsiei după un traumatism cerebral. Un studiu a constatat că PTE este mai frecventă la supraviețuitorii bărbați TBI decât la femei.
Istorie
Înregistrările PTE există încă din 3000 î.Hr. Trepanarea , în care este tăiată o gaură în craniu, ar fi putut fi folosită pentru a trata PTE în culturile antice. La începutul secolului al XIX-lea, chirurgii Baron Larrey și WC Wells au raportat fiecare că au efectuat operația pentru PTE. Chirurgul american cu educație franceză Benjamin Winslow Dudley (1785-1870) a efectuat șase trepanări pentru PTE între anii 1819 și 1832 în Kentucky și a avut rezultate bune în ciuda indisponibilității antisepsiei . Operația a presupus deschiderea craniului la locul rănirii, desbriderea țesutului rănit și, uneori, scurgerea sângelui sau a lichidului de sub dura mater . Munca lui Dudley a fost cea mai mare serie de acest gen care a fost făcută până în acel moment și a încurajat alți chirurgi să folosească trepanarea pentru convulsiile post-traumatice. Rapoartele sale despre operații au venit înainte de a fi acceptat că intervenția chirurgicală pentru ameliorarea excesului de presiune în craniu a fost eficientă în tratarea epilepsiei, dar a ajutat la stabilirea etapei trepanării pentru ca PTE să devină o practică obișnuită. Procedura a devenit mai acceptată la sfârșitul secolului al XIX-lea, odată ce antisepsia a fost disponibilă și localizarea cerebrală a fost un concept familiar. Cu toate acestea, în 1890, proeminentul medic german Ernest von Bergmann a criticat procedura; el și-a pus la îndoială eficacitatea (cu excepția unor circumstanțe particulare) și a sugerat că operațiunile au fost declarate reușite prea curând după proceduri pentru a ști dacă acestea vor conferi un beneficiu pe termen lung. La sfârșitul secolului al XIX-lea a apărut apariția chirurgiei intracraniene , care operează pe leziuni cerebrale despre care se crede că provoacă convulsii, un pas dincolo de chirurgia craniană care a implicat doar craniul și meningele . Până în 1893, cel puțin 42 de operații intracraniene au fost efectuate pentru PTE în SUA, cu succes limitat.
Chirurgia a fost tratamentul standard pentru PTE până în anii care au urmat celui de-al doilea război mondial, când afecțiunea a primit mai multă atenție pe măsură ce soldații care supraviețuiseră traumatismului cranian au dezvoltat-o. Nevoia crescută de medicamente pentru tratarea TEP a dus la studii cu antiepileptice; aceste studii timpurii au sugerat că medicamentele ar putea preveni epileptogeneza (dezvoltarea epilepsiei). Încă se credea că medicamentele antiepileptice ar putea preveni epileptogeneza în anii 1970; în 1973, 60% dintre medicii chestionați le-au folosit pentru a preveni PTE. Cu toate acestea, studiile clinice care au susținut un efect protector al antiepilepticelor au fost necontrolate; în studiile controlate ulterior, medicamentele nu au reușit să demonstreze un efect antiepileptogen. Studiile au arătat că antiepilepticele au împiedicat apariția convulsiilor în decurs de o săptămână după rănire și, în 1995, grupul de lucru al Brain Trauma Foundation a publicat o recomandare care sugerează utilizarea acestora pentru a proteja împotriva convulsiilor la începutul după traumatism. Cu toate acestea, au fost publicate recomandări împotriva utilizării profilactice a medicamentelor antiepileptice la mai mult de o săptămână după rănire de către grupul Brain Injury Special Interest al Academiei Americane de Medicină Fizică și Reabilitare în 1998 și de către Asociația Americană a Chirurgilor Neurologici în 2000.
Cercetare
Modul în care se dezvoltă epilepsia după o leziune a creierului nu este pe deplin înțeles și obținerea unei astfel de înțelegeri poate ajuta cercetătorii să găsească modalități de prevenire sau să o facă mai puțin severă sau mai ușor de tratat. Cercetătorii speră să identifice biomarkeri, indicații biologice că se produce epileptogeneza, ca mijloc de a găsi medicamente care pot viza căile prin care se dezvoltă epilepsia. De exemplu, medicamentele ar putea fi dezvoltate pentru a interfera cu leziunile cerebrale secundare (leziuni care nu apar în momentul traumei, dar rezultă din procesele inițiate de acesta), prin blocarea căilor, cum ar fi deteriorarea radicalilor liberi a țesutului cerebral. O creștere a înțelegerii diferențelor de vârstă în dezvoltarea epilepsiei după traume poate ajuta, de asemenea, cercetătorii să găsească biomarkeri ai epileptogenezei. Există, de asemenea, interes în găsirea mai multor medicamente antiepileptice, cu potențialul de a interfera cu epileptogeneza. Unele medicamente antiepileptice noi, cum ar fi topiramatul , gabapentina și lamotrigina, au fost deja dezvoltate și s-au dovedit promițătoare în tratamentul PTE. Niciun model animal nu are toate caracteristicile epileptogenezei la om, astfel încât eforturile de cercetare vizează identificarea unuia. Un astfel de model poate ajuta cercetătorii să găsească noi tratamente și să identifice procesele implicate în epileptogeneză. Cu toate acestea, cele mai frecvente modele mecanice de leziuni cerebrale traumatice, cum ar fi leziunile cu percuție lichidă, impactul cortical controlat și modelele de leziune prin scădere în greutate prezintă epileptogeneză în momente cronice cu convulsii documentate electroencefalografice și comportamentale la distanță și o susceptibilitate crescută a convulsiilor. S-a raportat că PTE poate apărea și la peștele zebră, rezultând răspunsuri fiziopatologice similare cu TBI umane.
Vezi si
Referințe
linkuri externe
| Clasificare | |
|---|---|
| Resurse externe |