Sulfat de potasiu - Potassium sulfate
 Arcanit
|
|
|
|
| Numele | |
|---|---|
| Alte nume
Sulfat de potasiu
|
|
| Identificatori | |
|
Model 3D ( JSmol )
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard |
100.029.013 |
| Numărul E | E515 (i) (regulatoare de aciditate, ...) |
| KEGG | |
|
PubChem CID
|
|
| Numărul RTECS | |
| UNII | |
|
Tablou de bord CompTox ( EPA )
|
|
|
|
|
|
| Proprietăți | |
| K 2 SO 4 | |
| Masă molară | 174,259 g / mol |
| Aspect | Solid alb |
| Miros | inodor |
| Densitate | 2,66 g / cm 3 |
| Punct de topire | 1.069 ° C (1.342 K) |
| Punct de fierbere | 1.689 ° C (3.072 ° F; 1.962 K) |
| 111 g / L (20 ° C) 120 g / L (25 ° C) 240 g / L (100 ° C) |
|
| Solubilitate | puțin solubilă în glicerol insolubilă în acetonă , alcool , CS 2 |
| −67,0 · 10 −6 cm 3 / mol | |
|
Indicele de refracție ( n D )
|
1.495 |
| Structura | |
| ortorombic | |
| Pericole | |
| Principalele pericole | Iritant |
| Fișa cu date de securitate | MSDS extern |
| Fraze R (învechite) | R22 |
| Fraze S (învechite) | S36 |
| Punct de aprindere | Neinflamabil |
| Doza sau concentrația letală (LD, LC): | |
|
LD 50 ( doza mediană )
|
6600 mg / kg (oral, șobolan) |
| Compuși înrudiți | |
|
Alți anioni
|
Selenat de potasiu Tellurat de potasiu |
|
Alți cationi
|
Sulfat de litiu Sulfat de sodiu Sulfat de rubidiu Sulfat de cesiu |
|
Compuși înrudiți
|
Hidrogen sulfat de potasiu sulfat de potasiu bisulfit de potasiu persulfat de potasiu |
|
|
|
| Referințe infobox | |
Sulfatul de potasiu (SUA) sau sulfatul de potasiu (Marea Britanie), numit și sulfat de potasiu (SOP), arcanit sau arhaic potasiu de sulf , este compusul anorganic cu formula K 2 SO 4 , un solid alb solubil în apă . Este frecvent utilizat în îngrășăminte , furnizând atât potasiu, cât și sulf .
Istorie
Sulfatul de potasiu (K 2 SO 4 ) este cunoscut de la începutul secolului al XIV-lea. A fost studiat de Glauber , Boyle și Tachenius. În secolul al XVII-lea, a fost numit arcanuni sau sal duplicatum , deoarece era o combinație dintr-o sare acidă cu o sare alcalină . De asemenea, a fost cunoscut sub numele de tartru vitriolic și sare Glaser sau sal polychrestum Glaseri după chimistul farmaceutic Christopher Glaser care l-a preparat și a folosit medicamentos.
Cunoscut sub numele de arcanum duplicatum („dublu secret”) sau panacea duplicata în medicina pre-modernă , a fost preparat din reziduul ( caput mortuum ) rămas din producția de aqua fortis (acid azotic, HNO 3 ) din nitru (azotat de potasiu, KNO 3 ) și ulei de vitriol (acid sulfuric, H 2 SO 4 ) prin procesul Glauber :
- 2 KNO 3 + H 2 SO 4 → 2 HNO 3 + K 2 SO 4
Reziduul a fost dizolvat în apă fierbinte, filtrat și evaporat până la o cuticulă. A fost apoi lăsat să cristalizeze. A fost folosit ca diuretic și sudorific .
Conform Ciclopediei Chambers , rețeta a fost achiziționată pentru cinci sute de taleri de Charles Frederick, Duce de Holstein-Gottorp . Schroder, medicul ducelui, a scris minuni despre marile sale utilizări în cazurile de ipohondriac , continuând și intermitând febre , piatră, scorbut și multe altele.
Resurse naturale
Forma minerală a sulfatului de potasiu, arcanitul , este relativ rară. Resursele naturale de sulfat de potasiu sunt minerale abundente în sarea Stassfurt . Acestea sunt cocristalizări de sulfat de potasiu și sulfate de magneziu , calciu și sodiu .
Mineralele relevante sunt:
- Kainită , KMG (SO 4 ) · Cl · 3H 2 O
- Schönite (acum cunoscută sub numele de picromerită), K 2 SO 4 · MgSO 4 · 6H 2 O
- Leonit , K 2 SO 4 · MgSO 4 · 4H 2 O
- Langbeinite , K 2 Mg 2 (SO 4 ) 3
- Aphtitalita (cunoscută anterior sub numele de glaserită), K 3 Na (SO 4 ) 2
- Polialit , K 2 SO 4 · MgSO 4 · 2CaSO 4 · 2H 2 O
Sulfatul de potasiu poate fi separat de unele dintre aceste minerale, cum ar fi kainita, deoarece sarea corespunzătoare este mai puțin solubilă în apă.
Kieserit , MgSO 4 · H 2 O, poate fi combinat cu o soluție de clorură de potasiu la sulfat produc potasiu.
Producție
Aproximativ 1,5 milioane de tone au fost produse în 1985, de obicei prin reacția clorurii de potasiu cu acidul sulfuric , analog procesului Mannheim pentru producerea sulfatului de sodiu. Procesul implică formarea intermediară de bisulfat de potasiu , o reacție exotermă care are loc la temperatura camerei:
- KCl + H 2 SO 4 → HCl + KHSO 4
Al doilea pas al procesului este endoterm, necesitând aport de energie:
- KCl + KHSO 4 → HCl + K 2 SO 4
Structură și proprietăți
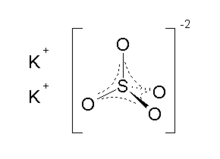
Sunt cunoscute două forme cristaline. Β-K 2 SO 4 ortorombic este forma comună, dar se convertește în α-K 2 SO 4 peste 583 ° C. Aceste structuri sunt complexe, deși sulfatul adoptă geometria tetraedrică tipică.
Nu formează un hidrat, spre deosebire de sulfatul de sodiu . Sarea cristalizează sub formă de piramide duble cu șase fețe, clasificate ca rombice. Sunt transparente, foarte dure și au un gust amar, sărat. Sarea este solubilă în apă, dar insolubilă în soluții de hidroxid de potasiu ( sp. Gr. 1.35) sau în etanol absolut .
Când sulfatul de potasiu este încălzit în apă și supus rotirii într-un pahar, cristalele formează o structură spirală cu mai multe brațe atunci când sunt lăsate să se depună.
Utilizări
Utilizarea dominantă a sulfatului de potasiu este ca îngrășământ . K 2 SO 4 nu conține clorură, care poate fi dăunătoare pentru unele culturi. Sulfatul de potasiu este preferat pentru aceste culturi, care includ tutunul și unele fructe și legume. Culturile care sunt mai puțin sensibile pot necesita în continuare sulfat de potasiu pentru o creștere optimă dacă solul acumulează clorură din apa de irigații.
Sarea brută este, de asemenea, utilizată ocazional la fabricarea sticlei. Sulfatul de potasiu este, de asemenea, utilizat ca reductor rapid în sarcinile de propulsie de artilerie . Reduce blitz-ul botului , flareback și suprapresiunea exploziei.
Este uneori folosit ca un mediu de explozie alternativ similar cu sifon în sablare , deoarece este mai greu și în mod similar solubil în apă.
Sulfatul de potasiu poate fi utilizat și în pirotehnie în combinație cu azotat de potasiu pentru a genera o flacără violetă .
Reacții
Acidificare
Sulfat acid de potasiu ( de asemenea , cunoscut sub numele de bisulfat de potasiu), KHSO 4 , este ușor de produs prin reacția K 2 SO 4 cu acid sulfuric . Formează piramide rombice , care se topesc la 197 ° C (387 ° F). Se dizolvă în trei părți de apă la 0 ° C (32 ° F). Cei de soluție se comportă mult ca în cazul în care cele două sale congeneri , K 2 SO 4 și H 2 SO 4 , au fost parte prezentă alături de una de alta necombinată; un exces de etanol precipită sulfatul normal (cu puțin bisulfat) cu restul de acid rămas.
Comportamentul sării uscate condensate este similar atunci când este încălzit la câteva sute de grade; acționează asupra silicaților , titanatelor etc., la fel ca acidul sulfuric care este încălzit dincolo de punctul său natural de fierbere. Prin urmare, este frecvent utilizat în chimia analitică ca agent de dezintegrare. Pentru informații despre alte săruri care conțin sulfat, consultați sulfatul .



