Radiochirurgie - Radiosurgery
| Radiochirurgie | |
|---|---|
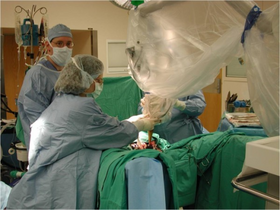 Fotografie intraoperatorie care prezintă poziționarea unui sistem de radiochirurgie. Pacientul din fotografie este tratat pentru cancer de rect.
| |
| Specialitate | Oncologie |
| MedlinePlus | 007577 |
| eMedicină | 1423298 |
Radiochirurgia este o intervenție chirurgicală care utilizează radiații , adică distrugerea anumitor zone ale țesutului folosind radiații ionizante, mai degrabă decât excizia cu o lamă. Ca și alte forme de radioterapie (numită și radioterapie), este de obicei utilizat pentru tratarea cancerului . Radiochirurgia a fost inițial definită de neurochirurgul suedez Lars Leksell ca „o fracție cu doză mare de radiații, direcționată stereotactic către o regiune intracraniană de interes”.
În radiochirurgia stereotactică ( SRS ), cuvântul „ stereotactic ” se referă la un sistem tridimensional de coordonate care permite corelarea precisă a unei ținte virtuale văzute în imaginile de diagnostic ale pacientului cu poziția țintă reală a pacientului. Radiochirurgia stereotactică poate fi numită și radioterapie stereotactică corporală (SBRT) sau radioterapie stereotactică ablativă (SABR) atunci când este utilizată în afara sistemului nervos central (SNC).
Istorie
Radiochirurgia stereotactică a fost dezvoltată pentru prima dată în 1949 de neurochirurgul suedez Lars Leksell pentru a trata ținte mici din creier care nu erau supuse intervenției chirurgicale convenționale. Instrumentul stereotactic inițial pe care l-a conceput a folosit sonde și electrozi. Prima încercare de a înlocui electrozii cu radiație a fost făcută la începutul anilor cincizeci, cu raze x . Principiul acestui instrument a fost să atingă ținta intra-craniană cu fascicule înguste de radiații din mai multe direcții. Căile fasciculului converg în volumul țintă, oferind acolo o doză letală cumulativă de radiație, limitând în același timp doza la țesutul sănătos adiacent. Zece ani mai târziu s-au făcut progrese semnificative, datorate în mare măsură contribuției fizicienilor Kurt Liden și Börje Larsson. În acest moment, fasciculele de protoni stereotactici înlocuiseră razele X. Fasciculul de particule grele s-a prezentat ca un înlocuitor excelent pentru cuțitul chirurgical, dar sincrociclotronul era prea stângace. Leksell a început să dezvolte un instrument practic, compact, precis și simplu, care să poată fi manipulat chiar de chirurg. În 1968, acest lucru a dus la cuțitul Gamma, care a fost instalat la Institutul Karolinska și consta din mai multe surse radioactive de cobalt-60 plasate într-un fel de cască cu canale centrale pentru iradiere cu raze gamma. Acest prototip a fost conceput pentru a produce leziuni de radiație asemănătoare fantei pentru proceduri neurochirurgicale funcționale pentru a trata durerea, tulburările de mișcare sau tulburările de comportament care nu au răspuns la tratamentul convențional. Succesul acestei prime unități a dus la construirea unui al doilea dispozitiv, care conține 179 de surse de cobalt-60. Această a doua unitate Gamma Knife a fost concepută pentru a produce leziuni sferice pentru tratarea tumorilor cerebrale și a malformațiilor arteriovenoase intracraniene (AVM). Unități suplimentare au fost instalate în anii 1980, toate cu 201 de surse de cobalt-60.
În paralel cu aceste evoluții, a fost concepută o abordare similară pentru un accelerator liniar de particule sau Linac. Instalarea primului accelerator liniar clinic de 4 MeV a început în iunie 1952 în Unitatea de Cercetare Radioterapeutică Medical Research Council (MRC) de la Spitalul Hammersmith , Londra. Sistemul a fost predat pentru fizică și alte teste în februarie 1953 și a început să trateze pacienții la 7 septembrie acel an. Între timp, lucrările la Laboratorul de microunde Stanford au dus la dezvoltarea unui accelerator de 6 VM, care a fost instalat la Spitalul Universitar Stanford, California, în 1956. Unitățile Linac au devenit rapid dispozitive favorizate pentru radioterapia fracționată convențională, dar a durat până în anii 1980 înainte de a fi dedicată Radiochirurgia Linac a devenit o realitate. În 1982, neurochirurgul spaniol J. Barcia-Salorio a început să evalueze rolul radiochirurgiei cu fotoni generată de cobalt și apoi pe baza de Linac pentru tratamentul AVM și epilepsie . În 1984, Betti și Derechinsky au descris un sistem radiochirurgical bazat pe Linac. Winston și Lutz au avansat în continuare tehnologii de prototip radiochirurgical bazate pe Linac, încorporând un dispozitiv de poziționare stereotactic îmbunătățit și o metodă de măsurare a preciziei diferitelor componente. Folosind un Linac modificat, primul pacient din Statele Unite a fost tratat în Boston Brigham and Women's Hospital în februarie 1986.
secolul 21
Îmbunătățirile tehnologice în imagistica și calculul medical au condus la adoptarea clinică crescută a radiochirurgiei stereotactice și și-au extins domeniul de aplicare în secolul XXI. Acuratețea și precizia localizării care sunt implicite în cuvântul „stereotactic” rămân de cea mai mare importanță pentru intervențiile radiochirurgicale și sunt îmbunătățite semnificativ prin tehnologii de ghidare a imaginii , cum ar fi localizatorul N și localizatorul Sturm-Pastyr, care au fost inițial dezvoltate pentru chirurgia stereotactică .
În secolul 21, conceptul original de radiochirurgie s-a extins pentru a include tratamente cuprinzând până la cinci fracțiuni , iar radiochirurgia stereotactică a fost redefinită ca o disciplină neurochirurgicală distinctă care utilizează radiații ionizante generate extern pentru a inactiva sau eradica țintele definite, de obicei în cap sau coloană vertebrală, fără a fi nevoie de o incizie chirurgicală. Indiferent de asemănările dintre conceptele de radiochirurgie stereotactică și radioterapie fracționată, mecanismul de realizare a tratamentului este subtil diferit, deși ambele modalități de tratament au rezultate identice pentru anumite indicații. Radiochirurgia stereotactică are un accent mai mare pe administrarea de doze precise, mari în zone mici, pentru a distruge țesutul țintă, păstrând în același timp țesutul normal adiacent. Același principiu este urmat în radioterapia convențională, deși sunt mai susceptibile de a fi utilizate doze mai mici, răspândite pe zone mai mari (de exemplu, ca în tratamentele VMAT ). Radioterapia fracționată se bazează mai mult pe radiosensibilitatea diferită a țintei și a țesutului normal înconjurător la doza totală de radiații acumulată . Din punct de vedere istoric, domeniul radioterapiei fracționate a evoluat din conceptul original de radiochirurgie stereotactică după descoperirea principiilor radiobiologiei : reparație, reasortare, repopulare și reoxigenare. Astăzi, ambele tehnici de tratament sunt complementare, deoarece tumorile care pot fi rezistente la radioterapia fracționată pot răspunde bine la radiochirurgie, iar tumorile care sunt prea mari sau prea aproape de organele critice pentru o radiochirurgie sigură pot fi candidați potriviți pentru radioterapia fracționată.
Astăzi, atât programele de radiochirurgie Gamma Knife, cât și Linac sunt disponibile comercial în toată lumea. În timp ce cuțitul Gamma este dedicat radiochirurgiei, multe Linac sunt construite pentru radioterapie fracționată convențională și necesită tehnologie suplimentară și expertiză pentru a deveni instrumente dedicate de radiochirurgie. Nu există o diferență clară de eficacitate între aceste abordări diferite. Principalii producători, Varian și Elekta oferă Linacs dedicate radiochirurgiei, precum și mașini concepute pentru tratamentul convențional cu capacități de radiochirurgie. Sisteme concepute pentru a completa Linac-urile convenționale cu tehnologia de modelare a fasciculului, planificarea tratamentului și instrumente de ghidare a imaginii. Un exemplu de radiochirurgie dedicată Linac este CyberKnife , un Linac compact montat pe un braț robot care se deplasează în jurul pacientului și iradiază tumora dintr-un set mare de poziții fixe, imitând astfel conceptul Gamma Knife.
Aplicații clinice
Atunci când este utilizat în afara SNC, poate fi numit radioterapie stereotactică corporală (SBRT) sau radioterapie stereotactică ablativă (SABR).
Sistem nervos central
Radiochirurgia este efectuată de o echipă multidisciplinară de neurochirurgi , oncologi în radiații și fizicieni medicali pentru a opera și întreține instrumente extrem de sofisticate, extrem de precise și complexe, inclusiv acceleratori lineari medicali, unitatea Gamma Knife și unitatea Cyberknife. Iradierea extrem de precisă a țintelor din creier și coloană este planificată folosind informații din imagini medicale care sunt obținute prin tomografie computerizată , imagistică prin rezonanță magnetică și angiografie .
Radiochirurgia este indicată în primul rând pentru terapia tumorilor, a leziunilor vasculare și a tulburărilor funcționale. Cu această tehnică trebuie utilizată o apreciere clinică semnificativă, iar considerațiile trebuie să includă tipul leziunii, patologia dacă este disponibilă, dimensiunea, localizarea și vârsta și starea generală de sănătate a pacientului. Contraindicațiile generale la radiochirurgie includ o dimensiune excesiv de mare a leziunii țintă sau leziuni prea numeroase pentru tratament practic. Pacienții pot fi tratați în decurs de una până la cinci zile ca pacienți ambulatori . Prin comparație, șederea medie în spital pentru o craniotomie (neurochirurgie convențională, care necesită deschiderea craniului) este de aproximativ 15 zile. Rezultatul radiochirurgiei poate să nu fie evident decât la câteva luni după tratament. Deoarece radiochirurgia nu îndepărtează tumora, dar o inactivează biologic, lipsa de creștere a leziunii este considerată în mod normal a fi un succes al tratamentului. Indicațiile generale pentru radiochirurgie includ multe tipuri de tumori cerebrale, cum ar fi neuromele acustice , germinoamele , meningioamele , metastazele , nevralgia trigeminală, malformațiile arteriovenoase și tumorile bazei craniului, printre altele. Extinderea radioterapiei stereotactice la leziuni extracraniene este în creștere și include metastaze, cancer la ficat, cancer pulmonar, cancer pancreatic etc.
Mecanism de acțiune
Principiul fundamental al radiochirurgiei este cel al ionizării selective a țesuturilor, prin intermediul fasciculelor de radiații de mare energie. Ionizarea este producerea de ioni și radicali liberi care dăunează celulelor . Acești ioni și radicali, care pot fi formați din apa din celulă sau din materialele biologice, pot produce daune ireparabile ADN-ului, proteinelor și lipidelor, ducând la moartea celulei. Astfel, inactivarea biologică se efectuează într-un volum de țesut de tratat, cu un efect distructiv precis. Doza de radiație este de obicei măsurată în gri (un gri (Gy) este absorbția unui joule de energie pe kilogram de masă). O unitate care încearcă să ia în considerare atât diferitele organe care sunt iradiate, cât și tipul de radiație este sievertul , o unitate care descrie atât cantitatea de energie depusă, cât și eficiența biologică.
Riscuri
New York Times a raportat în decembrie 2010 că supradozajele de radiații au avut loc prin metoda acceleratorului liniar de radiochirurgie, datorată în mare parte unor măsuri de protecție inadecvate în echipamentele adaptate pentru radiochirurgia stereotactică. În SUA, Food and Drug Administration (FDA) reglementează aceste dispozitive, în timp ce cuțitul Gamma este reglementat de Comisia de reglementare nucleară .
Aceasta este dovada că imunoterapia poate fi utilă pentru tratamentul necrozei radiației în urma radioterapiei stereotactice.
Tipuri de surse de radiații
Selectarea tipului adecvat de radiație și dispozitiv depinde de mulți factori, inclusiv tipul leziunii, dimensiunea și locația în raport cu structurile critice. Datele sugerează că rezultatele clinice similare sunt posibile cu toate diversele tehnici. Mai importante decât dispozitivul utilizat sunt problemele privind indicațiile pentru tratament, doza totală administrată, programul de fracționare și conformitatea planului de tratament.
Cuțit Gamma
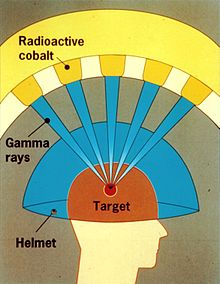
Un cuțit Gamma (cunoscut și sub numele de Cuțit Gamma Leksell) este utilizat pentru a trata tumorile cerebrale prin administrarea radioterapiei gamma de intensitate ridicată într-un mod care concentrează radiația pe un volum mic. Dispozitivul a fost inventat în 1967 la Institutul Karolinska din Stockholm , Suedia de către Lars Leksell, neurochirurgul român Ladislau Steiner și radiobiologul Börje Larsson de la Universitatea Uppsala , Suedia. Primul cuțit Gamma a fost adus în Statele Unite printr-un acord între neurochirurgul american Robert Wheeler Rand și Leksell și a fost dat Universității din California, Los Angeles (UCLA) în 1979.
Un cuțit Gamma conține de obicei 201 surse de cobalt-60 de aproximativ 30 de curii fiecare (1,1 TBq ), plasate într-o rețea emisferică într-un ansamblu puternic protejat . Dispozitivul vizează radiațiile gamma printr-un punct țintă din creierul pacientului. Pacientul poartă o cască specializată care este fixată chirurgical de craniu, astfel încât tumoarea cerebrală să rămână staționară în punctul țintă al razelor gamma. Prin urmare, o doză ablativă de radiație este trimisă prin tumoare într-o singură sesiune de tratament, în timp ce țesuturile cerebrale din jur sunt relativ scutite.
Terapia Gamma Knife, la fel ca toate radiochirurgia, utilizează doze de radiații pentru a distruge celulele canceroase și a micșora tumorile, administrate tocmai pentru a evita deteriorarea țesutului cerebral sănătos. Radiochirurgia Gamma Knife este capabilă să concentreze cu precizie mai multe fascicule de radiații gamma pe una sau mai multe tumori. Fiecare fascicul individual are o intensitate relativ scăzută, deci radiația are un efect redus asupra țesutului cerebral intervenit și este concentrată doar la tumoarea însăși.
Radiochirurgia Gamma Knife s-a dovedit eficientă la pacienții cu tumori cerebrale benigne sau maligne cu dimensiuni de până la 4 cm (1,6 in), malformații vasculare , cum ar fi o malformație arteriovenoasă (AVM), durere și alte probleme funcționale. Pentru tratamentul nevralgiei trigemenului, procedura poate fi utilizată în mod repetat la pacienți.
Complicațiile acute în urma radiochirurgiei Gamma Knife sunt rare, iar complicațiile sunt legate de afecțiunea tratată.
Terapii pe bază de accelerator liniar
Un accelerator liniar (linac) produce raze X din impactul electronilor accelerați care lovesc o țintă z înaltă , de obicei tungsten. Procesul este, de asemenea, denumit „terapie cu raze X” sau „terapie cu fotoni”. Capul de emisie, sau " gantry ", este rotit mecanic în jurul pacientului într-un cerc complet sau parțial. Masa pe care se află pacientul, „canapeaua”, poate fi, de asemenea, mutată în pași liniari sau unghiulari mici. Combinația mișcărilor porticului și a canapelei permite planificarea computerizată a volumului de țesut care va fi iradiat. Dispozitivele cu o energie mare de 6 MeV sunt cele utilizate în mod obișnuit pentru tratamentul creierului, datorită adâncimii țintei. Diametrul fasciculului de energie care iese din capul de emisie poate fi ajustat la dimensiunea leziunii prin intermediul colimatoarelor . Acestea pot fi orificii interschimbabile cu diametre diferite, de obicei variate de la 5 la 40 mm în trepte de 5 mm, sau colimatori multilaterali, care constau dintr-un număr de pliante metalice care pot fi deplasate dinamic în timpul tratamentului pentru a forma fasciculul de radiație pentru a se conforma masa de ablat. Începând din 2017, Linac-urile au fost capabile să realizeze geometrii fasciculului extrem de înguste, cum ar fi 0,15 până la 0,3 mm. Prin urmare, ele pot fi utilizate pentru mai multe tipuri de intervenții chirurgicale care până acum au fost efectuate prin intervenții chirurgicale deschise sau endoscopice, cum ar fi pentru nevralgia trigemenului. Datele de urmărire pe termen lung au arătat că este la fel de eficientă ca ablația prin radiofrecvență, dar inferioară intervenției chirurgicale în prevenirea reapariției durerii.
Primele astfel de sisteme au fost dezvoltate de John R. Adler , profesor de neurochirurgie și radioterapie oncologică la Universitatea Stanford , și de Russell și Peter Schonberg la Schonberg Research și comercializate sub marca CyberKnife.
Terapia cu fascicul de protoni
Protonii pot fi utilizați și în radiochirurgie într-o procedură numită Proton Beam Therapy (PBT) sau terapia cu protoni . Protonii sunt extrasați din materialele donatoare de protoni de către un sincrotron sau ciclotron medical și sunt accelerați în tranzite succesive printr-o conductă sau cavitate circulară, evacuată, folosind magneți puternici pentru a-și modela drumul, până când ajung la energia necesară pentru a traversa doar un corp uman, de obicei aproximativ 200 MeV. Acestea sunt apoi eliberate spre regiune pentru a fi tratate în corpul pacientului, ținta de iradiere. În unele mașini, care furnizează protoni doar cu o anumită energie, o mască personalizată din plastic este interpusă între sursa fasciculului și pacientul pentru a regla energia fasciculului pentru a oferi gradul adecvat de penetrare. Fenomenul vârfului Bragg al protonilor expulzați oferă avantaje în terapia cu protoni față de alte forme de radiații, deoarece cea mai mare parte a energiei protonului este depusă la o distanță limitată, astfel încât țesutul dincolo de acest interval (și într-o oarecare măsură și țesutul din acest interval) este scutit din efectele radiațiilor. Această proprietate a protonilor, care a fost numită „ efectul de încărcare a adâncimii ” prin analogie cu armele explozive utilizate în războiul antisubmarin, permite crearea unor distribuții conformale ale dozelor în jurul țintelor chiar cu formă foarte neregulată și pentru doze mai mari față de țintele înconjurate sau oprit de structuri sensibile la radiații, cum ar fi chiasma optică sau trunchiul cerebral. Dezvoltarea tehnicilor de „intensitate modulată” a permis obținerea unor conformități similare utilizând radiochirurgia acceleratorului liniar.
Începând cu 2013 nu au existat dovezi că terapia cu protoni este mai bună decât orice alte tipuri de tratament în majoritatea cazurilor, cu excepția unui „pumn de cancere pediatrice rare”. Criticii, răspunzând numărului tot mai mare de instalații PBT foarte scumpe, au vorbit despre o „ cursă a înarmărilor medicale ” și „medicină nebună și politici publice nesustenabile”.
Referințe
linkuri externe
- Tratarea tumorilor care se mișcă cu carte de respirație pe radiochirurgie la ținte în mișcare (iulie 2007)
- Cartea de radiochirurgie în formă de fascicul pe radiochirurgie bazată pe LINAC folosind colimarea multilală (martie 2011)


