Sumatriptan - Sumatriptan
 | |
 | |
| Date clinice | |
|---|---|
| Denumiri comerciale | Imitrex, Imigran, alții |
| AHFS / Drugs.com | Monografie |
| Date despre licență | |
| Căi de administrare |
Pe cale orală , injecție subcutanată , spray nazal, electroforeză transdermică |
| Codul ATC | |
| Statut juridic | |
| Statut juridic | |
| Date farmacocinetice | |
| Biodisponibilitate | 15% (pe gură) / 96% (sc) |
| Legarea proteinelor | 14-21% |
| Metabolism | MAO |
| Timp de înjumătățire prin eliminare | 2,5 ore |
| Excreţie | 60% urină ; 40% fecale |
| Identificatori | |
| |
| Numar CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| CompTox Dashboard ( EPA ) | |
| ECHA InfoCard |
100.130.518 |
| Date chimice și fizice | |
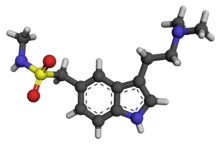
| Formulă | C 14 H 21 N 3 O 2 S |
| Masă molară | 295,40 g · mol −1 |
| Model 3D ( JSmol ) | |
| |
| |
| (verifica) | |
Sumatriptanul , vândut sub numele de marca Imitrex, printre altele, este un medicament utilizat pentru a trata durerile de cap de migrenă și durerile de cap în grup . Se ia pe cale orală, în nas sau prin injectare sub piele . Efectele apar în general în decurs de trei ore.
Efectele secundare frecvente includ presiunea toracică , oboseala, vărsăturile, furnicăturile și senzația că lumea se învârte. Efectele secundare grave pot include sindromul serotoninei , atacurile de cord , accidentele vasculare cerebrale și convulsiile . În cazul utilizării excesive a medicamentelor, pot apărea dureri de cap . Nu este clar dacă utilizarea în timpul sarcinii sau alăptării este sigură. Cum funcționează nu este pe deplin clar. Se află în clasa de medicamente triptan .
Sumatriptanul a fost brevetat în 1982 și aprobat pentru uz medical în 1991. Se află pe lista medicamentelor esențiale a Organizației Mondiale a Sănătății . Este disponibil ca medicament generic . În 2018, a fost a 111-a medicație cea mai frecvent prescrisă în Statele Unite, cu peste 6 milioane de rețete. Este, de asemenea, disponibil ca produs combinat sumatriptan / naproxen .
Utilizări medicale
Sumatriptanul este eficient pentru eliminarea sau ameliorarea intensității migrenei și a durerilor de cap . Este cel mai eficient atunci când este luat devreme după începerea durerii. Sumatriptanul injectat este mai eficient decât alte formulări.
Sumatriptanul oral poate fi utilizat și în tratamentul durerii de cap cu puncție post-durală.
Efecte adverse
Supradozajul cu sumatriptan poate provoca sulfhemoglobinemie , o afecțiune rară în care sângele se schimbă de la roșu la verde, datorită integrării sulfului în molecula de hemoglobină . Dacă sumatriptanul este întrerupt, starea se inversează în câteva săptămâni.
Evenimente cardiace grave, inclusiv unele care au fost fatale, au apărut în urma utilizării injecției cu sumatriptan sau a comprimatelor. Evenimentele raportate au inclus vasospasmul arterei coronare , ischemia miocardică tranzitorie, infarctul miocardic , tahicardia ventriculară și fibrilația ventriculară .
Cele mai frecvente reacții adverse raportate de cel puțin 2% dintre pacienți în studiile controlate cu sumatriptan (comprimate de 25, 50 și 100 mg) pentru migrenă sunt senzațiile atipice (parestezii și senzații de căldură / frig) raportate cu 4% în grupul placebo și 5-6% în grupurile sumatriptan, durerea și alte senzații de presiune (inclusiv durerea toracică) raportate cu 4% în grupul placebo și 6-8% în grupurile sumatriptan, evenimente neurologice ( vertij ) raportate cu mai puțin de 1 % în grupul placebo și mai puțin de 1% până la 2% în grupurile cu sumatriptan. Oboseala / oboseala a apărut la mai puțin de 1% din grupul placebo și 2-3% din grupurile cu sumatriptan. Tulburările de somn au apărut la mai puțin de 1% în grupul placebo, până la 2% în grupul cu sumatriptan.
Mecanism de acțiune
Sumatriptanul este similar din punct de vedere structural cu serotonina (5-HT) și este un receptor 5-HT (tipuri 5-HT 1D și 5-HT 1B ) agonist . Cu toate acestea, efectul terapeutic primar al Sumatriptanului constă în inhibarea eliberării peptidei legate de gena Calcitoninei (CGRP), probabil prin acțiunea sa agonistă a receptorului 5-HT 1D / 1B . Acest lucru este confirmat de eficacitatea antagoniștilor și anticorpilor CGRP nou dezvoltați în tratamentul preventiv al migrenei. Cu toate acestea, modul în care agonismul receptorilor 5-HT 1D / 1B inhibă eliberarea CGRP nu este pe deplin înțeles. Se crede că CGRP provoacă sensibilizarea neuronilor nociceptivi trigemen, contribuind la durerea experimentată în migrenă.
Sumatriptanul arată, de asemenea, că scade activitatea nervului trigemen , ceea ce presupune probabil eficacitatea sumatriptanului în tratarea durerilor de cap cluster. S-a demonstrat că forma injectabilă a medicamentului întrerupe durerea de cap în 30 de minute în 77% din cazuri.
Farmacocinetica
Sumatriptanul se administrează în mai multe forme: tablete, injecție subcutanată și spray nazal. Administrarea orală (ca sare succinată ) suferă de biodisponibilitate slabă , parțial din cauza metabolismului presistemic - unele dintre acestea se descompun în stomac și în fluxul sanguin înainte de a ajunge la arterele țintă. O nouă formulare cu tabletă cu eliberare rapidă are aceeași biodisponibilitate, dar concentrația maximă este atinsă în medie cu 10-15 minute mai devreme. Când este injectat, sumatriptanul acționează mai rapid (de obicei în decurs de 10 minute), dar efectul durează mai scurt. Sumatriptanul este metabolizat în principal de monoaminooxidază A în acid 2- {5 - [(metilsulfamoil) metil] -indol-3-il} acetic, care este apoi conjugat cu acid glucuronic . Acești metaboliți sunt excretați în urină și bilă. Doar aproximativ 3% din medicamentul activ poate fi recuperat nemodificat.
Nu există o relație simplă și directă între concentrația de sumatriptan (farmacocinetică) în sine în sânge și efectul său anti-migrenă (farmacodinamică). Acest paradox a fost, într-o oarecare măsură, rezolvat comparând ratele de absorbție ale diferitelor formulări de sumatriptan, mai degrabă decât cantitățile absolute de medicament pe care le furnizează.
Istorie
Aprobare
În 1991, Glaxo a primit aprobarea pentru sumatriptan, care a fost primul triptan disponibil . În Statele Unite, este disponibil numai pe bază de rețetă medicală (și este frecvent limitat, fără autorizație prealabilă, la o cantitate de nouă într-o perioadă de 30 de zile). Această cerință pentru o rețetă medicală există și în Australia. Cu toate acestea, poate fi cumpărat de la ghișeu în Marea Britanie și Suedia. Au fost aprobate mai multe forme de dozare pentru sumatriptan, inclusiv tablete , soluție injectabilă și inhalatoare nazale .
În iulie 2009, FDA din SUA a aprobat o formulare cu jet de unică folosință a sumatriptanului. Dispozitivul administrează o injecție subcutanată de 6 mg sumatriptan, fără utilizarea unui ac. Autoinjectoarele cu ace au fost disponibile anterior în Europa și America de Nord de câțiva ani.
Studiile de faza III , cu un iontoforetic plasture transdermic (Zelrix / Zecuity) a început în iulie 2008. Acest patch utilizează joasă tensiune controlat printr - un pre-programat microcip pentru a furniza o singură doză de sumatriptan prin piele în decurs de 30 de minute. Zecuity a fost aprobat de FDA din SUA în ianuarie 2013. Vânzările de Zecuity au fost oprite în urma raportărilor de arsuri și iritații ale pielii.
Generice
Brevetele Glaxo pentru sumatriptan au expirat în februarie 2009. În acel moment, Imitrex se vândea cu aproximativ 25 USD pe pastilă. La 6 noiembrie 2008, Par Pharmaceutical a anunțat că va începe să livreze imediat la comerț versiuni generice de injecție de sumatriptan (injecție de succinat de sumatriptan) kituri de start de 4 și 6 mg și cartușe de seringă umplute de 4 și 6 mg. În plus, Par anticipează lansarea flacoanelor de 6 mg la începutul anului 2009.
Mylan Laboratories Inc. , Ranbaxy Laboratories , Sandoz (o filială a Novartis ), Dr. Reddy’s Laboratories și alte companii au primit aprobarea FDA pentru versiunile generice de comprimate de sumatriptan în doze de 25, 50 și 100 mg din 2009. medicamentul este disponibil în mod generic pe piețele SUA și europene, deoarece protecția brevetelor Glaxo a expirat în acele jurisdicții. Sprayul nazal sumatriptan este, de asemenea, disponibil generic.
Statut juridic
În Rusia, versiunile sumatriptanului, care nu sunt înregistrate în registrul național al medicamentelor, pot fi considerate droguri narcotice (derivați ai dimetiltriptaminei ).
Referințe
linkuri externe
- „Sumatriptan” . Portalul de informații despre droguri . Biblioteca Națională de Medicină din SUA.

