Boala Wilson - Wilson's disease
| Boala Wilson | |
|---|---|
| Alte nume | Boala Wilson, degenerescenta hepatolenticulară |
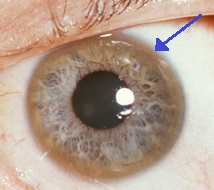 | |
| Un inel maro pe marginea irisului ( inelul Kayser – Fleischer ) este comun în boala Wilson, mai ales atunci când sunt prezente simptome neurologice. | |
| Specialitate | Gastroenterologie |
| Simptome | Umflarea picioarelor , pielea gălbuie , modificări de personalitate |
| Debut obișnuit | Vârsta cuprinsă între 5 și 35 de ani |
| Cauze | Genetic |
| Diagnostic diferentiat | Boală hepatică cronică , boala Parkinson , scleroză multiplă , altele |
| Tratament | Modificări dietetice, agenți de chelare , suplimente de zinc , transplant de ficat |
| Frecvență | ~ 1 la 30.000 |
Boala Wilson este o tulburare genetică în care excesul de cupru se acumulează în organism. Simptomele sunt de obicei legate de creier și ficat . Simptomele legate de ficat includ vărsături , slăbiciune, acumulare de lichid în abdomen , umflarea picioarelor , pielea gălbuie și mâncărime . Simptomele legate de creier includ tremurături , rigiditate musculară, probleme de vorbire, modificări ale personalității, anxietate și psihoză .
Boala Wilson este cauzata de o mutatie in proteina boala Wilson ( ATP7B ) gena . Această proteină transportă excesul de cupru în bilă , unde este excretat în deșeuri. Condiția este autozomală recesivă ; pentru ca o persoană să fie afectată, trebuie să moștenească o copie mutată a genei de la ambii părinți. Diagnosticul poate fi dificil și implică adesea o combinație de teste de sânge, teste de urină și o biopsie hepatică . Testarea genetică poate fi utilizată pentru a depista membrii familiei celor afectați.
Boala Wilson este tratată de obicei cu modificări dietetice și medicamente. Modificările dietetice implică consumul unei diete cu conținut scăzut de cupru și nu utilizarea vaselor de cupru. Medicamentele utilizate includ agenți de chelare, cum ar fi trientină și d-penicilamină și suplimente de zinc . Complicațiile bolii Wilson pot include insuficiență hepatică , cancer hepatic și probleme renale . Un transplant de ficat poate fi util la cei la care alte tratamente nu sunt eficiente sau dacă apare insuficiență hepatică.
Boala Wilson apare la aproximativ 1 din 30.000 de persoane. Simptomele încep de obicei între 5 și 35 de ani. A fost descris pentru prima dată în 1854 de patologul german Friedrich Theodor von Frerichs și poartă numele neurologului britanic Samuel Wilson .
semne si simptome
Principalele locuri de acumulare a cuprului sunt ficatul și creierul și, în consecință, bolile hepatice și simptomele neuropsihiatrice sunt principalele caracteristici care conduc la diagnostic. Persoanele cu probleme hepatice tind să vină la asistență medicală mai devreme, în general ca copii sau adolescenți, decât cei cu simptome neurologice și psihiatrice, care tind să aibă vârsta de douăzeci sau mai mari. Unele sunt identificate doar pentru că rudelor le-a fost diagnosticată boala Wilson; multe dintre acestea, atunci când sunt testate, se dovedesc a fi avut simptome ale afecțiunii, dar nu au primit un diagnostic.
Boală de ficat
Boala hepatică se poate prezenta ca oboseală , tendință crescută de sângerare sau confuzie (datorită encefalopatiei hepatice ) și hipertensiune portală . Acesta din urmă, o afecțiune în care presiunea din vena portală este semnificativ crescută, duce la varice esofagiene , vase de sânge în esofag care pot sângera în mod periculos, precum și mărirea splinei ( splenomegalie ) și acumularea de lichid în cavitatea abdominală ( ascită ). La examinare, pot fi observate semne de boli hepatice cronice, cum ar fi paianjenul angiomat (mici vase de sânge distinse, de obicei pe piept). Hepatita cronică activă a cauzat ciroză hepatică în majoritatea timpului în care dezvoltă simptome. În timp ce majoritatea persoanelor cu ciroză prezintă un risc crescut de carcinom hepatocelular (cancer la ficat), acest risc este relativ foarte scăzut în boala Wilson.
Aproximativ 5% din toate persoanele sunt diagnosticate numai atunci când dezvoltă insuficiență hepatică acută fulminantă , adesea în contextul unei anemii hemolitice (anemie datorată distrugerii globulelor roșii). Acest lucru duce la anomalii în producția de proteine (identificate prin coagulare deranjată ) și metabolismul de către ficat. Metabolismul proteic deranjat duce la acumularea de produse reziduale, cum ar fi amoniacul în sânge. Când acestea irită creierul , persoana dezvoltă encefalopatie hepatică (confuzie, coma, convulsii și, în cele din urmă, umflarea creierului care pune viața în pericol ).
Simptome neuropsihiatrice
Aproximativ jumătate dintre persoanele cu boala Wilson au simptome neurologice sau psihiatrice. Majoritatea au inițial deteriorări cognitive ușoare și stângăcie, precum și modificări de comportament. Apare apoi de obicei simptome neurologice specifice, adesea sub formă de parkinsonism (rigiditatea roții dințate, bradikinezie sau mișcări încetinite și lipsa de echilibru sunt cele mai frecvente trăsături parkinsoniene) cu sau fără tremor tipic de mână , expresii faciale mascate, vorbire neclară, ataxie ( lipsa coordonării) sau distonie (mișcări răsucite și repetitive ale unei părți a corpului). Convulsiile și migrenele par a fi mai frecvente în boala Wilson. Un tremur caracteristic descris ca „tremur de aripi” este întâlnit la mulți oameni cu Wilson; aceasta este absentă în repaus, dar poate fi provocată prin răpirea brațelor și flexarea coatelor spre linia mediană.
Cognitia poate fi afectata si in boala Wilson. Aceasta apare în două categorii, care nu se exclud reciproc, tulburări ale lobului frontal (pot apărea ca impulsivitate , afectare a judecății, promiscuitate , apatie și disfuncție executivă, cu o planificare și luare a deciziilor slabe) și demență subcorticală (pot apărea ca gândire lentă, pierdere de memorie și executivă disfuncție , fără semne de afazie , apraxia sau agnozie ). Se sugerează că aceste implicări cognitive sunt legate și strâns legate de manifestările psihiatrice ale bolii.
Problemele psihiatrice datorate bolii Wilson pot include modificări de comportament, depresie , tulburări de anxietate și psihoză . Simptomele psihiatrice sunt frecvent observate împreună cu simptomele neurologice și rareori se manifestă singure. Aceste simptome sunt adesea slab definite și uneori pot fi atribuite altor cauze. Din această cauză, diagnosticul bolii Wilson este rar pus atunci când sunt prezente doar simptome psihiatrice.
Alte sisteme de organe
Condițiile medicale au fost corelate cu acumularea de cupru în boala Wilson:
- Ochi: Inelele Kayser – Fleischer ( inele KF), un semn patognomonic , pot fi vizibile în corneea ochilor, fie direct, fie la examinarea lămpii cu fante ca depuneri de cupru într-un inel din jurul corneei. Acestea se datorează depunerii de cupru din membrana lui Descemet . Aceste inele pot fi maro închis, auriu sau verde-roșcat, au o lățime de 1 până la 3 mm și apar la limbul corneei. Nu apar la toate persoanele cu boala Wilson. Boala Wilson este, de asemenea, asociată cu cataracta de floarea-soarelui, prezentată prin pigmentarea maro sau verde a capsulei cristalinului anterior și posterior. Nici unul nu provoacă pierderi vizuale semnificative. Inelele KF apar în aproximativ 66% din cazurile diagnosticate (mai des în cele cu simptome neurologice, mai degrabă decât cu probleme hepatice).
- Rinichi: acidoză tubulară renală (tip 2), o tulburare a manipulării bicarbonatului de către tubii proximali duce la nefrocalcinoză (acumularea de calciu în rinichi), o slăbire a oaselor (datorită pierderii de calciu și fosfat) și, ocazional, aminoacidurie (pierderea aminoacizi necesari pentru sinteza proteinelor).
- Inima: cardiomiopatia (slăbiciunea mușchiului inimii) este o problemă rară, dar recunoscută în boala Wilson; poate duce la insuficiență cardiacă (acumularea de lichid datorită scăderii funcției pompei) și aritmii cardiace (episoade de ritm cardiac neregulat și / sau anormal de rapid sau lent).
- Hormoni: hipoparatiroidism (eșecul glandelor paratiroide care duc la niveluri scăzute de calciu), infertilitate și avort spontan recurent .
Genetica
Gena bolii Wilson ( ATP7B ) se află pe cromozomul 13 (13q14.3) și se exprimă în principal în ficat, rinichi și placentă . Gena codifică o ATPază de tip P (enzimă de transport cationic) care transportă cuprul în bilă și îl încorporează în ceruloplasmină . Mutațiile pot fi detectate în 90% din cazuri. Majoritatea (60%) sunt homozigoți pentru mutațiile ATP7B (două copii anormale), iar 30% au o singură copie anormală. Zece la sută nu au mutații detectabile.
Deși au fost descrise 300 de mutații ale ATP7B , în majoritatea populațiilor cazurile de boală Wilson se datorează unui număr mic de mutații specifice acelei populații. De exemplu, la populațiile occidentale mutația H1069Q (înlocuirea unei histidine cu o glutamină la poziția 1069 în proteină) este prezentă în 37-63% din cazuri, în timp ce în China această mutație este foarte neobișnuită și R778L ( arginină la leucină la 778 ) se găsește mai des. Se știe relativ puțin despre impactul relativ al diferitelor mutații, deși mutația H1069Q pare să prezică debutul ulterior și problemele predominant neurologice, potrivit unor studii. O resursă completă adnotată clinic, WilsonGen oferă clasificare clinică pentru variante conform recomandărilor recente ACMG și AMP
O variație normală a genei PRNP poate modifica evoluția bolii prin întârzierea vârstei de debut și afectarea tipului de simptome care se dezvoltă. Această genă produce proteină prionică , care este activă în creier și în alte țesuturi și, de asemenea, pare să fie implicată în transportul cuprului. Un rol pentru gena ApoE a fost inițial suspectat, dar nu a putut fi confirmat.
Condiția este moștenită într-un model autosomal recesiv. Pentru a o moșteni, ambii părinți ai unei persoane trebuie să poarte o genă afectată. Majoritatea nu au antecedente familiale ale afecțiunii. Persoanele cu o singură genă anormală sunt numite purtători (heterozigoți) și pot prezenta anomalii ușoare, dar nesemnificative din punct de vedere medical, ale metabolismului cuprului.
Boala Wilson este cea mai frecventă dintr-un grup de boli ereditare care cauzează supraîncărcarea cuprului în ficat. Toate pot provoca ciroza la o vârstă fragedă. Ceilalți membri ai grupului sunt ciroză indiană pentru copii (ICC), ciroză infantilă tiroleză endemică și toxicoză idiopatică de cupru. Acestea nu sunt legate de mutațiile ATP7B : de exemplu, ICC a fost legată de mutațiile genei KRT8 și KRT18 .
Fiziopatologie

Cuprul este necesar de către organism pentru o serie de funcții , predominant ca cofactor pentru mai multe enzime precum ceruloplasmină, citocrom c oxidază , dopamină β-hidroxilază , superoxid dismutază și tirozinază .
Cuprul pătrunde în organism prin tractul digestiv . O proteină transportoare de pe celulele intestinului subțire , membrană de cupru transportor 1 (Ctr1; SLC31A1), transportă cuprul în interiorul celulelor, unde unele sunt legate de metalotioneină, iar o parte este transportată de ATOX1 către un organet cunoscut sub numele de rețeaua trans-Golgi . Aici, ca răspuns la creșterea concentrațiilor de cupru, o enzimă numită ATP7A (proteina Menkes) eliberează cupru în vena portă în ficat. Celulele hepatice transportă, de asemenea, proteina CMT1, iar metalotioneina și ATOX1 o leagă în interiorul celulei, dar aici este ATP7B care leagă cuprul de ceruloplasmină și îl eliberează în sânge, precum și îndepărtarea excesului de cupru secretând-o în bilă . Ambele funcții ale ATP7B sunt afectate de boala Wilson. Cuprul se acumulează în țesutul hepatic; ceruloplasmina este încă secretată, dar într-o formă lipsită de cupru (denumită apoceruloplasmină) și care se degradează rapid în fluxul sanguin.
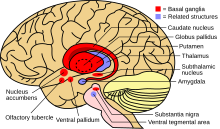
Când cantitatea de cupru din ficat copleșește proteinele care îl leagă în mod normal, provoacă leziuni oxidative printr-un proces cunoscut sub numele de chimia Fenton ; această afectare duce în cele din urmă la hepatită cronică activă , fibroză (depunerea țesutului conjunctiv) și ciroză . Ficatul eliberează de asemenea cupru în fluxul sanguin care nu este legat de ceruloplasmină. Acest cupru liber precipită pe tot corpul, în special în rinichi, ochi și creier. În creier, cea mai mare parte a cuprului se depune în ganglionii bazali , în special în putamen și globus pallidus (numiți împreună nucleul lenticular ); aceste zone participă în mod normal la coordonarea mișcării, precum și joacă un rol semnificativ în procesele neurocognitive, cum ar fi procesarea stimulilor și reglarea dispoziției. Deteriorarea acestor zone, din nou de către chimia Fenton, produce simptomele neuropsihiatrice observate în boala Wilson.
Nu este clar de ce boala Wilson provoacă hemoliză, dar diferite linii de dovezi sugerează că un nivel ridicat de cupru liber (care nu este legat de ceruloplasmină ) are un efect direct asupra oxidării hemoglobinei , inhibării enzimelor care furnizează energie în celulele roșii din sânge. , sau deteriorarea directă a membranei celulare .
Diagnostic
Boala Wilson poate fi suspectată pe baza oricărui simptom menționat mai sus sau atunci când s-a constatat că o rudă apropiată are Wilson. Majoritatea au teste funcționale hepatice ușor anormale , cum ar fi un nivel ridicat de aspartat transaminazic , alanină transaminază și bilirubină . Dacă afectarea ficatului este semnificativă, albumina poate fi scăzută din cauza incapacității celulelor hepatice deteriorate de a produce această proteină; în mod similar, timpul de protrombină (un test de coagulare ) poate fi prelungit deoarece ficatul este incapabil să producă proteine cunoscute ca factori de coagulare. Nivelurile de fosfatază alcalină sunt relativ scăzute la cei cu insuficiență hepatică acută legată de Wilson. Dacă există simptome neurologice, se realizează de obicei imagistica prin rezonanță magnetică (RMN) a creierului; aceasta prezintă hiperintensități în partea creierului numită ganglionii bazali în cadrul T2 . RMN poate demonstra, de asemenea, modelul caracteristic „fața panda uriaș” .
Nu există un test total fiabil pentru boala Wilson, dar nivelurile de ceruloplasmină și cupru din sânge, precum și cantitatea de cupru excretată în urină într-o perioadă de 24 de ore, sunt utilizate împreună pentru a forma o impresie a cantității de cupru din corpul. Standardul de aur -sau cel mai ideal test este o biopsie hepatica .
Ceruloplasmin
Nivelurile de ceruloplasmină sunt anormal de scăzute (<0,2 g / L) în 80-95% din cazuri. Cu toate acestea, poate fi prezent la niveluri normale la persoanele cu inflamație continuă , deoarece este o proteină de fază acută . Ceruloplasmina scăzută se găsește și în boala Menkes și aceruloplasminemia , care sunt înrudite, dar mult mai rare decât boala Wilson.
Combinația de simptome neurologice, inele Kayser-Fleischer și un nivel scăzut de ceruloplasmină este considerată suficientă pentru diagnosticul bolii Wilson. Cu toate acestea, în multe cazuri, sunt necesare teste suplimentare.
Cupru din ser și urină
Cuprul seric este scăzut, ceea ce poate părea paradoxal, având în vedere că boala Wilson este o boală a excesului de cupru. Cu toate acestea, 95% din cuprul plasmatic este transportat de ceruloplasmină, care este adesea scăzută în boala Wilson. Cuprul din urină este crescut în boala Wilson și este colectat timp de 24 de ore într-o sticlă cu o căptușeală fără cupru. Nivelurile peste 100 μg / 24h (1,6 μmol / 24h) confirmă boala Wilson, iar nivelurile peste 40 μg / 24h (0,6 μmol / 24h) sunt puternic orientative. Nivelurile ridicate de cupru în urină nu sunt unice pentru boala Wilson; acestea sunt uneori observate în hepatita autoimună și în colestază (orice boală care obstrucționează fluxul de bilă de la ficat la intestinul subțire).
La copii, poate fi utilizat testul penicilaminei . Se administrează o doză orală de 500 mg de penicilamină, iar urina se colectează timp de 24 de ore. Dacă acesta conține mai mult de 1600 μg (25 μmol), acesta este un indicator fiabil al bolii Wilson. Acest test nu a fost validat la adulți.
Biopsie hepatică
Odată ce alte investigații au indicat boala Wilson, testul ideal este îndepărtarea unei cantități mici de țesut hepatic printr-o biopsie hepatică . Acest lucru este evaluat microscopic pentru gradul de steatoză și ciroză , iar histochimia și cuantificarea cuprului sunt utilizate pentru a măsura severitatea acumulării de cupru. Un nivel de 250 μg de cupru pe gram de țesut hepatic uscat confirmă boala Wilson. Ocazional, se găsesc niveluri mai scăzute de cupru; în acest caz, combinația rezultatelor biopsiei cu toate celelalte teste ar putea duce în continuare la un diagnostic formal al lui Wilson.
În stadiile anterioare ale bolii, biopsia prezintă de obicei steatoză (depunere de material gras), glicogen crescut în nucleu și zone de necroză (moarte celulară). În boala mai avansată, modificările observate sunt destul de similare cu cele observate în hepatita autoimună, cum ar fi infiltrarea de către celulele inflamatorii , necroza bucală și fibroza (țesutul cicatricial). În boala avansată, în cele din urmă, ciroza este principala constatare. În insuficiența hepatică acută, se observă degenerarea celulelor hepatice și colapsul arhitecturii țesutului hepatic, de obicei pe un fond de modificări cirotice. Metodele histochimice pentru detectarea cuprului sunt incoerente și nesigure, și luate singure sunt considerate insuficiente pentru a stabili un diagnostic.
Testarea genetică
Se poate efectua analiza mutației genei ATP7B , precum și a altor gene legate de acumularea de cupru în ficat. Odată ce o mutație este confirmată, este posibil să se examineze membrii familiei pentru boală ca parte a consilierii familiale de genetică clinică . Distribuțiile regionale ale genelor asociate cu boala Wilson sunt importante de urmat, deoarece acest lucru poate ajuta clinicienii să proiecteze strategii adecvate de screening. Deoarece mutațiile genei WD variază între populații, cercetările și testele genetice efectuate în țări precum SUA sau Regatul Unit pot pune probleme, deoarece tind să aibă populații mai mixte.
Tratament
Dietă
În general, se recomandă o dietă săracă în alimente care conțin cupru, evitând ciuperci , nuci , ciocolată , fructe uscate , ficat, semințe de susan și ulei de susan și crustacee .
Medicament
Sunt disponibile tratamente medicale pentru boala Wilson. Unele cresc îndepărtarea cuprului din corp, în timp ce altele împiedică absorbția cuprului din dietă.
În general, penicilamina este primul tratament utilizat. Aceasta leagă cuprul ( chelarea ) și duce la excreția cuprului în urină. Prin urmare, monitorizarea cantității de cupru în urină se poate face pentru a se asigura o doză suficient de mare. Penicilamina nu este lipsită de probleme: aproximativ 20% prezintă un efect secundar sau o complicație a tratamentului cu penicilamină, cum ar fi lupusul indus de medicamente (care provoacă dureri articulare și erupții cutanate) sau miastenia (o afecțiune nervoasă care duce la slăbiciune musculară). La cei care au prezentat simptome neurologice, aproape jumătate prezintă o agravare paradoxală a simptomelor lor. În timp ce acest fenomen este observat în alte tratamente pentru Wilson, este de obicei luat ca o indicație pentru întreruperea penicilaminei și începerea tratamentului de linia a doua. Cei intoleranți la penicilamină pot începe în schimb cu clorhidrat de trientină , care are, de asemenea, proprietăți chelatoare. Unii recomandă trientina ca tratament de primă linie, dar experiența cu penicilamina este mai extinsă. Un alt agent, aflat sub investigație clinică de către Wilson Therapeutics , cu activitate cunoscută în boala Wilson este tetrathiomolibdatul . Acest lucru este considerat experimental, deși unele studii au arătat un efect benefic.
Odată ce toate rezultatele au revenit la normal, zincul (de obicei sub formă de rețetă de acetat de zinc numită Galzin) poate fi utilizat în locul chelatorilor pentru a menține niveluri stabile de cupru în organism. Zincul stimulează metalotioneina , o proteină din celulele intestinale care leagă cuprul și previne absorbția și transportul acestora în ficat. Terapia cu zinc este continuată, cu excepția cazului în care simptomele se repetă sau dacă excreția urinară de cupru crește.
În cazuri rare în care niciunul dintre tratamentele orale nu este eficient, în special în cazul bolilor neurologice severe, este necesară ocazional dimercaprol (anti-Lewisite britanic). Acest tratament este injectat intramuscular (într-un mușchi) la fiecare câteva săptămâni și are efecte secundare neplăcute, cum ar fi durerea.
Oamenii care sunt asimptomatici (de exemplu, cei diagnosticați prin screening familial sau numai ca urmare a rezultatelor anormale ale testelor) sunt în general tratați, deoarece acumularea de cupru poate provoca daune pe termen lung în viitor. Nu este clar dacă aceste persoane sunt tratate cel mai bine cu penicilamină sau acetat de zinc.
Terapii fizice și ocupaționale
Fizioterapia și terapia ocupațională sunt benefice pentru pacienții cu forma neurologică a bolii. Tratamentul chelator cu cupru poate dura până la șase luni pentru a începe să lucreze, iar aceste terapii pot ajuta la gestionarea ataxiei , distoniei și tremurăturilor, precum și la prevenirea dezvoltării contracturilor care pot rezulta din distonie.
Transplantul
Transplantul de ficat este un remediu eficient pentru boala Wilson, dar este utilizat numai în anumite scenarii din cauza riscurilor și complicațiilor asociate cu procedura. Este utilizat în principal la persoanele cu insuficiență hepatică fulminantă care nu răspund la tratament medical sau la cei cu boli hepatice cronice avansate. Transplantul hepatic este evitat în cazul bolilor neuropsihiatrice severe, în care beneficiul acestuia nu a fost demonstrat.
Prognoză
Lăsată netratată, boala Wilson tinde să se înrăutățească progresiv și în cele din urmă este fatală. Cu detectarea și tratamentul precoce, majoritatea celor afectați pot trăi o viață relativ normală. Afectarea hepatică și neurologică care apare înainte de tratament se poate îmbunătăți, dar este adesea permanentă.
Istorie
Boala poartă numele medicului britanic Samuel Alexander Kinnier Wilson (1878-1937), un neurolog care a descris starea, inclusiv modificările patologice din creier și ficat, în 1912. Lucrarea lui Wilson a fost precedată de și a atras, rapoartele neurologului german Carl Westphal (în 1883), care a numit-o „pseudoscleroză”; de neurologul britanic William Gowers (în 1888); de neuropatologul finlandez Ernst Alexander Homén (în 1889–1892), care a remarcat caracterul ereditar al bolii; și de Adolph Strümpell (în 1898), care a remarcat ciroza hepatică. Neuropatologul John Nathaniel Cumings a făcut legătura cu acumularea de cupru atât în ficat, cât și în creier în 1948. Apariția hemolizei a fost observată în 1967.
În 1951, Cumings și neurologul din Noua Zeelandă, Derek Denny-Brown , care lucrează în Statele Unite, au raportat simultan primul tratament eficient, folosind chelator metalic anti-Lewisite britanic . Acest tratament a trebuit să fie injectat, dar a fost una dintre primele terapii disponibile în domeniul neurologiei, domeniu care în mod clasic a fost capabil să observe și să diagnosticheze, dar a avut puține tratamente de oferit. Primul agent eficient de chelare orală, penicilamina , a fost descoperit în 1956 de neurologul britanic John Walshe. În 1982, Walshe a introdus și trientina și a fost primul care a dezvoltat tetrathiomolibdat pentru uz clinic. Terapia cu acetat de zinc și-a făcut apariția inițial în Olanda, unde medicii Schouwink și Hoogenraad au folosit-o în 1961 și, respectiv, în anii 1970, dar a fost dezvoltată ulterior de Brewer și colegii de la Universitatea din Michigan .
Baza genetică a bolii Wilson și legătura acesteia cu mutațiile ATP7B a fost elucidată de mai multe grupuri de cercetare în anii 1980 și 1990.
Alte animale
Acumularea ereditară de cupru a fost descrisă în Bedlington Terriers , unde în general afectează numai ficatul. Se datorează mutațiilor genei COMMD1 (sau MURR1 ). În ciuda acestor descoperiri, mutațiile COMMD1 nu au putut fi detectate la oameni cu stări de acumulare de cupru non-wilsonian (cum ar fi ciroza indiană din copilărie ) pentru a explica originea genetică a acestora.
Vezi si
Referințe
linkuri externe
- Boala Wilson la Curlie
- Boala Wilson la NLM Genetics Home Reference
| Clasificare | |
|---|---|
| Resurse externe |